Somatex VERTEBROPLASTY User manual

GEBRAUCHSANWEISUNG
INSTRUCTIONS FOR USE
MODE D‘UTILISATION
ΟΔΗΓΙΕΣ ΧΡΗΣΕΩΣ
ISTRUZIONI D’USO
MANUAL DE INSTRUÇŐES
MODO DE EMPLEO
ИНСТРУКЦИЯ ДЛЯ ПРИМЕНЕНИЯ
NÁVOD K POUŽITÍ
VERTEBROPLASTIE
REF: 999844V6 – 08-2014
1 2 3 4 5 6
2/32
3
5
4
21
6
Click
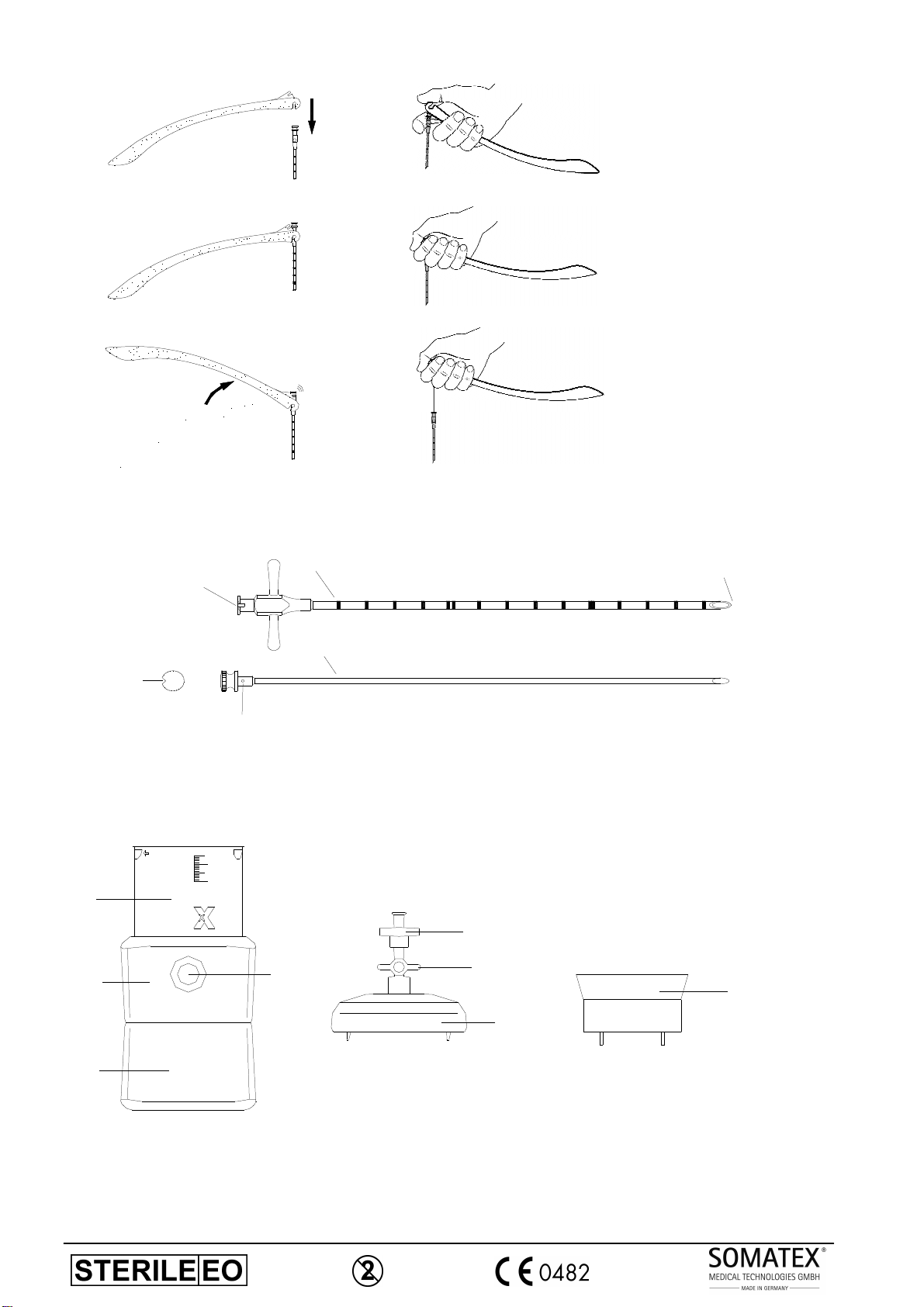
Abb. 2 a-f, Nadelhalter / needle holder
Abb.3, Vertebroplastie-Kanüle / Vertebroplasty cannula
SOMATE
II.
I.
III. IV.
V.
VI.
VII.
VIII.
Abb.4, Mischsystem Überblick / Mixing device overview
a)
b)
c)
d)
e)
f)
3/32
7 8
STOP
1 2
SOMATE
9
10 11 12
OFF
3 4 5
2.1.
SOMATE
CLICK
6
2.
OFF ON
1.
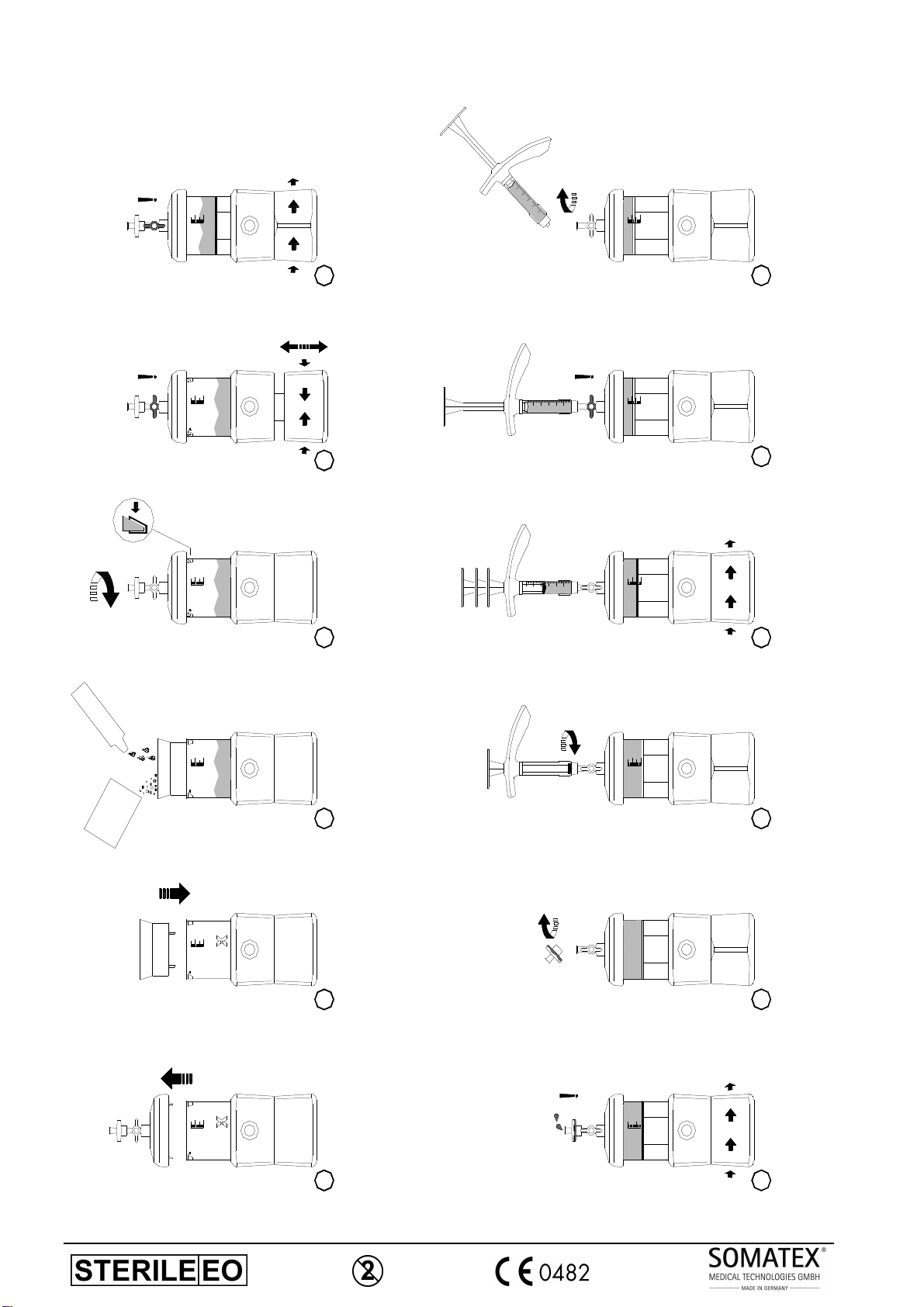
Abb.5, Mischsystem Abfolge / mixing device sequence
4/32
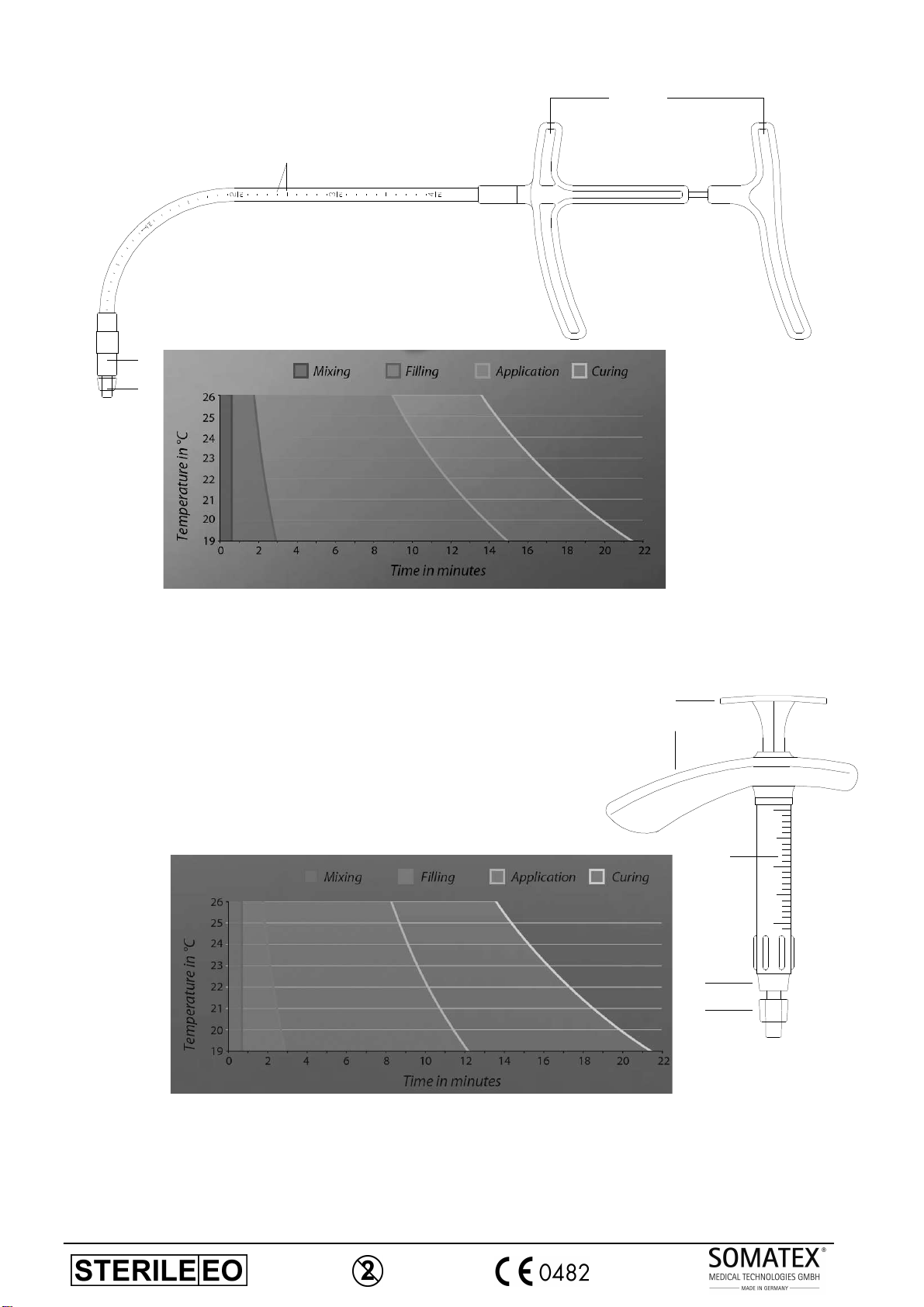
Abb.6, Injektionssystem CIS
®
mit Verarbeitungszeiten / injection device CIS
®
with working phases
Abb.7, Injektionssystem SIS mit Verarbeitungszeiten / injection device SIS with working phases
3
2
1
1
2
3
4
4
1
2
3

5/32
Gebrauchsanweisung (German)
Dieses Instrument wurde ausdrücklich für den einmaligen Gebrauch hergestellt. Das Produkt darf nach einmaliger Anwendung nicht
wieder verwendet werden. Die Qualität der Materialien, Beschichtungen und Klebeverbindungen können sich verschlechtern. Eine
sichere Anwendung ist nicht mehr gewährleistet. Das Produkt ist nach einmaliger Verwendung nicht für die notwendigen Reinigungs-
und Sterilisierungsprozesse ausgelegt. Die Sterilität der wiederaufbereiteten Einmalprodukte ist somit nicht gewährleistet. Das Risiko
von ungewollten Verletzungen und Infektionen, insbesondere Kreuzinfektionen bei Patient und medizinischem Personal steigt
unangemessen. Die Firma Somatex lehnt jede Verantwortung im Falle einer Resterilisation und Wiederverwendung des Instrumentes
ab.
Diese Anweisung für SOMATEX
®
Vertebroplastie-Sets hat NICHT den Zweck, medizinische oder chirurgische Methoden festzulegen
oder vorzuschlagen. Der jeweilige Arzt ist für die Festlegung der geeigneten Verfahren und Methoden in Verbindung mit der
Anwendung dieses Produktes verantwortlich.
1. Indikation:
Die VERTEBROPLASTIE dient zur Stabilisierung der Wirbelkörperstruktur mit Knochenzement zur Behandlung von schmerzhaften,
pathologischen Wirbelkörperkompressionsfrakturen, die nicht durch eine konservative Schmerztherapie behandelt werden können
und gekennzeichnet sind durch:
- primäre und sekundäre Osteoporose,
- Osteolysen aus Tumoren im Wirbelkörper (metastasierende Karzinome oder Myelome),
- Osteolysen aus symptomatischen Wirbelkörperhämangiomen.
Es ist darauf hinzuweisen, dass Wirbelkörperaugmentations-Verfahren nur palliative Behandlungen zur Stabilisierung der
Wirbelkörper und der Schmerzen sind. Sie behandeln nicht die zugrunde liegende Krankheit (Osteoporose oder Tumor-
Erkrankungen).
Die VERTEBROPLASTIE ist nicht geeignet, um als Prophylaxe bei osteoporotischen Patienten mit oder ohne Wirbelkörperfrakturen
eingesetzt zu werden.
2. Kontraindikationen
Wenden Sie keine VERTEBROPLASTIE an wenn bekannt ist, dass der Patient eine Überempfindlichkeit gegenüber den
Bestandteilen des Sets und/oder des Knochenzements mit Kontrastmittel hat.
Absolute Kontraindikationen:
- Schwangerschaft oder Stillzeit
- nicht vollständig geklärte lokale oder systemische Infektionen
- nicht steuerbare hämorrhagische Krankheiten
Relative Kontraindikationen:
- in den Epiduralraum erweiterte Tumore des Wirbelkörpers
- Wirbelkörpertumore, die den Spinalkanal betreffen und mehr als 20% des Wirbels einnehmen
- Berstungsfrakturen innerhalb der Wirbelsäule
- anatomischer Wirbelkörperschaden, verursacht durch unsicheren Zugang zum Wirbelkörper
- mangelnde Zusammenarbeit des Patienten bzw. Patienten, die nicht in der Lage sind, den Anweisungen des medizinischen
Personals Folge zu leisten
- Stoffwechselerkrankungen, die die Polymerisationsreaktion des Knochenzements stören
- Osteomalazie
- nicht lokale Infektionen, die potentiell den Wirbelkörper betreffen können
- Hypotonie
- Herzinsuffizienz
- Nierenversagen
3. Produktbeschreibung
(Abb.1, Deckblatt)
Das Somatex
®
VERTEBROPLASTIE - Set ist ein steriles Einweg-Produkt, das zur Injektion von Knochenzement durch eine Kanüle in
den Wirbelkörper dient. Je nach Variante besteht es aus einer oder zwei Kanülen (1) zur mono- oder bilateralen Punktion, einem
Nadelhalter (2) zur Führung der Kanülen außerhalb des Strahlengangs, einem Mischbecher mit Spatel (4) oder einem Mischsystem
(3) und einem oder zwei kleinen Injektionsspritzen (SIS) (5) oder einem Injektionssystem (CIS
®
) (6). Alle Sets (Tab.2) können mit dem
in der Liste aufgeführten Zubehör (Tab.3) ergänzt werden.
4. Warnhinweise
- Unmittelbar während und nach einer Vertebroplastie sollte der Blutdruck des Patienten sorgfältig auf Veränderungen monitoriert
werden. Unerwünschte Reaktionen des Herz-Kreislauf-Systems des Patienten können bei der Anwendung von Augmentationen
auftreten. Hypotone Reaktionen können zwischen 5 Sekunden und mehreren Minuten nach der Anwendung von Knochenzement
andauern. In seltenen Fällen kann es zum Herzstillstand kommen. Deshalb sollten die Patienten unmittelbar nach der
Anwendung von Knochenzement sorgfältig hinsichtlich der Vitalfunktionen überwacht werden.
- In seltenen Fällen sind im Zusammenhang mit einer Vertebroplastie schwere Nebenwirkungen wie Myokardinfarkt, Herzstillstand,
Schlaganfall und Lungenembolie aufgetreten.
- Im Falle einer Komplikation des Lungen-, Herz- oder Kreislaufsystems ist es notwendig, einen kontrollierten Zustand und eine
angemessene Volämie wieder herzustellen.
- Im Falle einer akuten Atem- oder Herzinsuffizienz oder Reanimation muss mit geeigneten Techniken für die Aufrechterhaltung
der lebenswichtigen Funktionen gesorgt werden.
- Vor der Implantation von Knochenzement ist es notwendig, Risiken oder Kontraindikation auszuschließen. (siehe auch absolute
und relative Kontraindikationen). Insbesondere sollte eine genaue Kontrolle der Morphologie des gebrochenen Wirbelkörpers,
mögliche Vaskularisierung oder das Vorhandensein von Ödemen durch geeignete bildgebende Verfahren durchgeführt werden.
- Vor einer Vertebroplastie sollten Schutzmaßnahmen geschaffen werden, durch einen sofortigen chirurgischen Eingriff etwaige
Komplikationen zu korrigieren.
- Die Punktion des Knochens mit der Vertebroplastie-Kanüle muss mit Hilfe eines geeigneten bildgebenden Verfahren erfolgen, um
den korrekten Sitz der Kanülenspitze zu überprüfen.
- Es ist zwingend notwendig, vertebrale Augmentationen unter Echtzeitbedingungen bei Röntgendurchleuchtung durchzuführen,
um die Verteilung von Knochenzement in der gesamten Ausdehnung des Wirbelkörpers zu sehen und der Anwender das
Auslaufen des Zements außerhalb des Wirbelkörpers vermeidet.
GERMAN

6/32
- Unzureichend gefüllte Wirbelkörper können unter Umständen die Symptome nicht vollständig korrigieren und langfristig
verminderte Stabilität der behandelten Wirbel bedeuten.
- Im Falle einer Knochenzementleckage außerhalb des Wirbelkörpers können paravertebrale Strukturen beschädigt werden und
möglicherweise Kompression des Rückenmarks, interkostale Schmerzen, Leckagen in den Zwischenwirbelraum, Füllungen
perivertebraler Blutgefäße mit der Gefahr einer Embolie, Infektionen und post-operative Schmerzen bedeuten.
- Während des Anmischens des Knochenzements ist vorsichtig zu sein und streng den Anweisungen des Herstellers zu folgen.
- Es sind die allgemeinen Vorschriften zu beachten, die das Verhalten und den Umgang mit medizinischen Instrumenten im sterilen
Bereich regeln.
- Kombinieren Sie das SOMATEX
®
Vertbroplastie-Set mit keinen anderen Komponenten als denen, die in der Liste als Zubehör
angegeben sind.
5. Anwendung
5.1 Kanüle, Nadelhalter und Vorbereitung:
1. Versichern Sie sich vor dem Gebrauch, dass die Verpackung nicht geöffnet und/oder beschädigt ist und überprüfen Sie das
Sterildatum, ob die Größe der Kanüle den Angaben auf dem Etikett entspricht und alle Komponenten vorhanden sind.
2. Die zu behandelnde Rückenpartie ist zu desinfizieren, der Wirbelkörper zu markieren und der Bereich steril abzudecken.
3. Ggf. ist eine Stichinzision an der Punktionsstelle mit einem Skalpell vor zu nehmen, um die Penetration der Haut zu erleichtern
4. Die Kanüle ist gemäß Abb. 2 a-c mit dem Nadelhalter zu konnektieren. Er dient zur Reduktion der Strahlenexposition der Hand
des Operateurs während der Punktion. Zusätzlich kann er zur leichteren Entfernung des Mandrins (Abb. 2 d-f) oder analog der
gesamten Kanüle verwendet werden.
5. Die Vertebroplastie-Kanüle (Abb.3) mit dem distalen Ende (1) ansetzen und vorsichtig in das Gewebe einbringen. Unter
radiologischer Sicht die Kanüle soweit vorbringen, bis ein Widerstand durch Wirbelkörperkontakt spürbar wird. Die Markierung (2)
dient zur Orientierung der Penetrationstiefe.
6. Nun die Kanüle vorsichtig im Knochen fixieren ggf. mittels leichter Hammerschläge. Wenn die Kanüle sicher positioniert ist, kann
der Nadelhalter entfernt werden. Es ist darauf zu achten, dass das Mandrin (4) vollständig im Luer-Anschluss (3) sitzt und durch
den Pin (5) gegen Verdrehen gesichert ist.
7. Die Lage der Kanülenspitze (1) und die korrekte Angulation unter CT/DSA-Kontrolle überprüfen und ggf. korrigieren. Eine
Kerbmarkierung am Stilettansatz (6) zeigt die Position der Nadelspitze an. Diese soll bei notwendigen Richtungskorrekturen die
Orientierung erleichtern.
8. Nach Ausrichtung in korrekte Position die Kanüle durch leichte und gezielte Hammerschläge weiter in den Wirbelkörper
hineintreiben. Zwischenzeitlich müssen weitere Positions-/ bzw. Richtungskontrollen bei geeigneter Bildgebung durchgeführt
werden.
Kanülendurchmesser in mm/G Kanülenlänge in mm Innenvolumina in ml ** passende Biopsiekanüle
3,00 / 11 100 0,45 2,0 / 14 x 150
3,00 / 11 125 0,55 2,0 / 14 x 200
3,00 / 11 150 0,65 2,0 / 14 x 200
2,50 / 12,5 125 0,31 -
2,00 / 14 125 0,24 -
Tab.1, KanülenDimensionen
** ca.-Werte gelten ausschließlich für SOMATEXVertebroplastie-Kanülen
Bei der Entnahme eines Biopsats über die Vertebroplastiekanüle ist auf die korrekte Dimensionierung (Tab.1) der Biopsiekanüle zu
achten und der Gebrauchsanweisung zu folgen.
5.2 Vorbereiten des Zements:
Es sind die Anweisungen des Zementherstellers zu beachten, insbesondere die Lager- und Temperaturhinweise und die
Verarbeitungszeiten. Je nach Variante ist das Set mit einem Mischsystem (Abb.1.3) oder einem Mischbecher mit Spatel (Abb 1.4)
ausgestattet.
a) Mischen mit Becher und Spatel
1. Füllen Sie die pulverförmige und die flüssige Komponente des Knochenzements in den Becher. Achten Sie darauf, dass beide
Verpackungen vollständig in den Becher entleert werden.
2. Vermischen Sie die Komponenten mit Hilfe des Spatels zu einer homogenen Masse. Dieser Vorgang sollte für ca. 1 Minute
kontinuierlich fortgeführt werden, um eine gleichmäßige Konsistenz zu erreichen.
b) Mischen mit Mischsystem (SOMIX 2.0), Abb. 4 und 5
BEFÜLLEN:
1. Drehen Sie den Verschlussdeckel des SOMIX
®
2.0 entgegen dem Uhrzeigersinn von der Kammer ab. (1) Dieser Schritt entfällt
beim ‚complete’-Set.
2. Setzen Sie den Trichter so auf die Kammer, dass er zentrisch und umlaufend anliegt. (2)
3. Befüllen Sie die Kammer zunächst mit dem Pulver und dann mit der Flüssigkeit. Achten Sie darauf, dass beide
Komponentenmengen vollständig entleert werden und nichts verschüttet wird. (3) Anschließend den Trichter wieder entfernen.
4. Schließen Sie die Mischkammer, indem der Verschlussdeckel im Uhrzeigersinn aufgeschraubt wird, bis ein deutliches Einrasten
zu spüren ist. Auf der Kammer angebrachte Markierungen zeigen den korrekten Verschluss. (4)
MISCHEN:
5. Kontrollieren Sie, ob der Hahn geschlossen ist. Bewegen Sie den unteren Griff zügig durch Schub- und Zugbewegungen.
Dadurch wird das Paddel in der Mischkammer auf und ab bewegt und sorgt für eine homogene Durchmischung. Zusätzliche
Drehbewegungen des Griffs können den Mischvorgang beschleunigen (5).
Um eine vollständige Mischung zu garantieren, wird empfohlen, den Vorgang kontinuierlich für mind. 30-40 Sekunden
durchzuführen. Die Konsistenz ist durch die transparente Mischkammer zu überprüfen.
Bei Bedarf kann über den Luer-Lock-Anschluss ein Unterdruck angeschlossen werden. In diesem Fall muss der Hahn geöffnet
sein.
GERMAN

7/32
TRANSFERIEREN
6. Öffnen Sie zunächst den Hahn. Schrauben Sie den unteren Griff im vollständig zusammengeschobenen Zustand gegen den
Uhrzeigersinn. (6) Hierdurch wird die Kammer entlüftet.
7. Stoppen Sie den Vorgang, wenn der Kammerboden den Beginn der Skalierung erreicht hat und der Zement den Hahn und den
Filter befüllt. (7)
8. Entfernen Sie den Filter durch Abschrauben gegen den Uhrzeigersinn. (8)
9. Setzen Sie das zu befüllende Injektionssystem oder die Spritze so auf, dass eine dichte Verbindung entsteht. (9)
10. Durch weiteres Schrauben des unteren Griffs wird der Zement in das Injektionssystem transferiert, bis es gefüllt ist. Der Kolben
des Injektionssystems hebt sich normalerweise von alleine. Der Fortschritt wird mit deutlichen Rastgeräuschen signalisiert, 6
‚Clicks’ ergeben eine 360°-Drehung. (10)
11. Entlasten Sie die Mischkammer vom Druck durch Drücken des Knopfes und/oder Schließen Sie den 2-Wege-Hahns. (11)
12. Entfernen Sie das Injektionssystem vom Hahn durch Drehen gegen den Uhrzeigersinn. (12)
13. Wiederholen Sie die Vorgänge 9 bis 12 solange, bis Sie genügend Injektionssysteme befüllt haben oder die Mischkammer
entleert ist.
•Konstruktionsbedingt verbleibt immer eine geringe Menge der Zementmischung in der Kammer und kann nicht transferiert
werden. In der Regel reicht die zur Verfügung stehende Zementmenge völlig aus.
•Der Zement sollte nach dem Mischen so schnell wie möglich in Spritzen oder Injektionssysteme transferiert werden, da die
zunehmende Viskosität den Transfer erschwert. In Abhängigkeit des Zementsverhaltens stehen hierfür 2-4 Min. zur Verfügung.
•Je nach Viskosität, Beschaffenheit und Konsistenz des Zements werden pro Klick ca. 0,2 ml ausgeworfen.
5.3 Injektionssysteme und Injektion
Cement Injection System (CIS®, Abb.6) und Small Injection System (SIS, Abb.7)
1. Griffe (4) zusammenschieben, Aufsaugstutzen (3) in den gemischten Zement halten und mindestens 3 ml (SIS 1 ml) Zement
aufziehen und komplett wieder in das Mischgefäß zurückgeben. Durch diesen Schritt wird sämtliche Luft aus dem
Injektionssystem
gedrückt. Beim Verwenden des Mischsystems wird der Ansaugstutzen nicht benötigt und das Injektionssystem
direkt mit 2-Wege-Hahn (Abb. 4.7) verbunden. Anschließend den Punkten 9-12 dieser Anleitung im Kapitel 6.2 folgen
2. Das Injektionssystem nun komplett auf die gewünschte Füllmenge aufziehen. Um das Einziehen von Luftblasen zu vermeiden
empfiehlt es sich, die Rührschüssel schräg zu halten und den Aufsaugstutzen (3) tiefstmöglich in den Zement einzutauchen.
3. Der Aufziehvorgang sollte mindestens fünf Sekunden betragen, da durch einen zu starken Sog Luftblasen wieder eingezogen
werden könnten. Die Genauigkeit der ml-Skala (1) beträgt ± 0,2 ml (CIS
®
) und ± 0,1 ml (SIS)
4. Vorsichtig das Mandrin (Abb. 5.4) aus der platzierten Kanüle entfernen. Das Mandrin muss im sterilen Bereich bleiben, da mit ihm
der Restzement aus der Kanüle in den Wirbelkörper gedrückt werden muss.
5. Aufsaugstutzen (3) vom Rotator (2) des Injektionssystems entfernen.
6. Luer-Lock des Injektionssystems auf die Kanüle (Abb. 3.3) fest aufschrauben.
7. Warten, bis der Zement die gewünschte Konsistenz hat.
8. Zementinjektion unter radiologischer Bildgebung. Hierbei muss unbedingt auf das Zeitfenster der Zementaushärtung geachtet
werden. Wenn nur noch mit größerer Kraftanstrengung Zement appliziert werden kann, sollte sofort mit dem nächsten Schritt
begonnen werden, da sonst ein Festzementieren der Kanüle droht.
Achtung: Übermäßige Kraftanwendung kann zu mechanischen Schäden am Injektionssystem führen.
9. Rotator des Injektionssystems von der Kanüle lösen.
10. Mandrin der Kanüle vollständig wieder in die Kanüle einführen und den Restzement aus Kanülenhohlraum in den Wirbelkörper
drücken. Die Tabelle (Tab.1) der Restvolumina der Somatex – Vertebroplastie-Kanülen befinden sich im entsprechenden Kapitel
der Gebrauchsanweisung.
11. Während der Aushärtungsphase des Zements die Kanüle in zeitlichen Abständen (30-60 sec.) wiederholt um 360° drehen, um
ein Festzementieren der Kanüle zu vermeiden.
Die Verarbeitungszeit des Zements ist vom Injektionssystem abhängig und gemäß den Diagrammen in Abb. 6 und 7 zu entnehmen.
5.4 Nachsorge
1.
Nach Aushärtung des Zements Kanüle mit der Hand durch Dreh/Zugbewegung aus dem Wirbelkörper entfernen. Gemäß Abb.2
a-f kann der Nadelhalter zum Entfernen der Kanüle zu Hilfe genommen werden.
2.
Wundstelle versorgen.
6. Lagerung und Entsorgung
Lagerungsanweisung:
Lagerung an einem dunklen, trockenen Platz (Luftfeuchtigkeit 30% - 65%) bei einer Temperatur zwischen 41°F - 86°F (5°C – 30°C).
Entsorgung:
Das Produkt kann nach der Verwendung gemäß den Vorschriften für klinischen Abfall entsorgt werden.
GERMAN

8/32
Instruction of use (English)
This tool is designed solely for disposable use. The product may not be re-used after a single application. The quality of materials,
coatings and adhesive joints may deteriorate. A secure application is no longer guaranteed. The product is not designed for cleaning
and sterilization processes after a single use. The sterility of reprocessed single-use is therefore not guaranteed. The risk of
unintentional injuries and infections, especially cross-infection with a patient and medical personnel increases inadequately. Somatex
does not accept any responsibility in the case of a reusing of this sterilised tool.
These instructions for Somatex
®
Vertebroplasty Set do NOT have the purpose of defining or proposing medical or surgical methods.
The concerned physician is responsible for the selection of the suitable procedures and methods relating to this product.
1. Indication:
VERTEBROPLASTY is used for stabilisation of the vertebral body using bone cement for treatment of painful pathological vertebral
body compression fractures that cannot be treated by a conventional palliative therapy and are marked by:
- Primary and secondary osteoporosis
- Osteolyses from tumours in the vertebral body (metastatic carcinomas or myelomas),
- Osteolyses from symptomatic vertebral haemangiomas.
It should be pointed out to the fact that vertebral augmentation procedures are only palliative treatments for stabilisation of the
vertebral body and the pains. They do not treat the causative disease (osteoporosis or tumour diseases).
VERTEBROPLASTY is not suitable for prophylactic treatment for osteoporotic patients with or without vertebral body fractures.
2. Contraindications
Do not apply VERTEBROPLASTY when the patient shows clear indication of hypersensitivity to the components of the set and/or the
bone cement with contrast agent.
Absolute Contraindications:
- Pregnancy or lactation period
- Incompletely clarified local or systemic infections
- Non-controllable haemorrhagic illnesses
Relative Contraindications:
- Tumours of the vertebral body extending to the epidural space
- Vertebral tumours that concern the spinal canal and occupy more than 20% of the vertebra
- Burst fractures within the spinal column
- Anatomical vertebral body injury caused by unsafe access to the vertebral body
- Lacking collaboration of the patient(s), who is/are not in a position to follow the instructions of the medical personnel
- Metabolic disorders that interrupt the polymerisation reaction of the bone cement
- Osteomalacia
- General infections that can potentially affect the vertebral body
- Hypotonia
- Cardiac insufficiency
- Kidney failure
3. Product Description
(Fig.1, cover sheet)
Somatex
®
VERTEBROPLASTY kit is a sterile disposable product that is used to inject bone cement through a cannula into the
vertebral body. According to the model, it consists of one or two cannulae (1) for mono or bilateral punctures, a needle holder (2) for
guiding the cannulae exterior to the beam path, a mixing bowl with spatula (4) or a mixer system (3) and one or two small injection
syringes (SIS) (5) or an injection system (CIS
®
) (6). All sets (Tab. 2) can be supplemented with the accessories itemised in the list
(Tab. 3).
4. Warning notices
- The blood pressure of the patient should be carefully monitored during and just after a vertebroplasty to observe any variations.
Adverse reactions of the cardiovascular system of the patient can appear during the application of augmentations. Hypotonic
reactions can last between 5 seconds and several minutes after the application of bone cement. In rare cases, it may lead to
cardiac arrest. Therefore, the patients should be carefully monitored with respect to the vital functions, just after the application of
bone cement.
- In rare cases, serious side-effects, such as myocardial infarct, cardiac arrest, stroke and pulmonary embolism may occur in the
context of vertebroplasty.
- In the case of a complication in the pulmonary, cardiac or cardiovascular system, it is necessary to establish a controlled
condition and appropriate volaemia.
- In the case of an acute respiratory or cardiac insufficiency or resuscitation, maintenance of the vital functions must be ensured
using suitable technologies.
- Before the implantation of bone cement, it is necessary to exclude risks or contraindication. (see also absolute and relative
contraindications). Especially, accurate inspection of the morphology of the broken vertebral body, possible vascularisation or the
existence of oedemas should be carried out through suitable imaging procedures.
- Before performing vertebroplasty, precautionary measures to correct any complications through an immediate surgical
intervention should be implemented.
- The puncture of the bone with the vertebroplasty cannula should be done by means of a suitable imaging procedure to check the
proper seating of the cannula tip.
- It is mandatory to carry out vertebral augmentations at real-time conditions under x-ray illumination, in order to see the distribution
of bone cement in the entire expansion of the vertebral body and the user prevents escape of the cement out of the vertebral
body.
- Insufficiently filled vertebral body may not correct the symptoms completely and can mean long-term diminished stability of the
treated vertebral body.
- In the case of a bone cement leakage outside the vertebral body, paravertebral structures can be damaged and can mean
possible compression of the spinal cord, intercostal pain, leakage in the intervertebral space, filling of perivertebral blood vessels
with the risk of an embolism, infections and post-operative pains.
- Caution should be exercised and the manufacturer’s instructions followed, while mixing the bone cement.
- The general instructions governing the behaviour and handling of medical instruments in the sterile area should be noted.
- Do not use the SOMATEX
®
Vertbroplasty Set together with any components, other than those indicated in the list as accessories.
- Caution: Federal (USA) Law restricts this device to sale by or on the order of a physician.
US /
ENG
LISH

9/32
5. Application
5.1 Cannula, Needle Holder and Preparation:
1. Prior to use, ensure that the packing is not opened and / or damaged; check the date of sterility expiration and whether the size of
the cannula corresponds to the specification on the label and all components are available.
2. The area of the back to be treated should be disinfected to mark the vertebral body and the area should be covered in a sterile
manner.
3. Where appropriate, a puncture incision should be done at the puncture site with a scalpel, in order to ease penetration into the
skin.
4. The cannula should be connected with the needle holder in accordance with Fig. 2 a-c. It is used to minimise the exposure of the
operator’s hand to radiation during the puncture. In addition, it can used for easier removal of the mandrel (Fig. 2 d-f) or similar to
the entire cannula.
5. Place the vertebroplasty cannula (Fig. 3) with the distal end (1) and insert carefully into the tissue. Viewing under radiological
illumination, push the cannula forward until resistance from the vertebral body is noticeable. The marking (2) is used for
orientation of the penetration depth.
6. Now, fix the cannula carefully in the bone or by exerting gentle hammer blows, where appropriate. The needle holder can be
removed when the cannula has been secured in place. It should be noted that that the mandrel (4) is housed completely in the
Luer connection (3) and is secured against turning by the pin (5).
7. Check the position of the cannula tip (1) and the correct angulation through CT/DSA inspection and correct, where appropriate. A
notch marking on the stiletto unit (6) indicates the position of the needle tip. This should ease orientation for the necessary
direction corrections.
8. After alignment in the correct position, move the cannula further into the vertebral body through gentle and targeted hammer
blows. Meanwhile, additional position and/or direction inspections should be carried out with suitable imaging.
Cannula diameter in mm/G
Cannula length in mm
Interior volume in ml **
Suitable biopsy cannula
3.00 / 11 100 0.45 2.0 / 14 x 150
3.00 / 11 125 0.55 2.0 / 14 x 200
3.00 / 11 150 0.65 2.0 / 14 x 200
2.50 / 12.5 125 0.31 -
2.00 / 14 125 0.24 -
Tab. 1 Cannula dimensions
** approximate values apply exclusively to SOMATEXVertebroplasty cannulae
When removing a biopsy over the vertebroplasty cannula, attention should be paid to the correct dimensioning (Tab. 1) of the biopsy
cannula and the instructions to use followed.
5.2 Preparing the Cement:
The instructions of the cement manufacturer should be followed, especially the warehouse and temperature instructions and the
processing times. According to the model, the set is equipped with a mixer system (Fig. 1.3) or a mixing bowl with spatula (Fig. 1.4).
a) Mixing with Bowl and Spatula
1. Fill the powdery and fluid component of the bone cement in the bowl. Ensure that both packs are emptied completely in the bowl.
2. Mix the components using the spatula to form a homogeneous mass. This process should be continuously carried out for about 1
minute to achieve uniform consistency.
b) mixing device for bone cement (SOMIX
®
2.0)
FILLING:
1. Turn on cap of SOMIX
®
2.0 from chamber counter clockwise. (1) This step is not applicable by ‘complete’ kits.
2. Put on funnel to chamber in a centrically and fitting way. (2)
3. Fill at first powder and following liquid into the chamber quickly. Pay attention that both components are filled in completely and
no amounts are spilled. (3) Afterwards remove the funnel.
4. Close chamber by turning cap clockwise till clear feel of latching. There are marks on chamber showing right position. (4)
MIXING:
5. Check if stopcock is closed. Move lower handle by pushing and pulling quickly. Thereby a paddle in chamber is moving up and
down and blending a homogenous mixture. In addition turning of lower handle will speed up mixing process. (5)
To assure a complete mixing is a continuous procedure recommended for at least 30-40 seconds.
Check consistency of bone cement via transparent chamber.
If demand vacuum can be provided by Luer-Lock-connector; in this case stopcock has to be open.
TRANSFER:
6. Open at first the stopcock. Turn lower handle counter clockwise in a pushed together position. (6) Thereby chamber will be
vented from air.
7. Stop the process if chamber bottom will reach beginning of scale and cement will fill stopcock and filter. (7)
8. Remove filter by turning counter clockwise. (8)
9. Connect an injection device or syringe to Luer-Lock-connector sealed. (9)
10. The cement will transferred into injection device by further handle turning till complete charging. The plunger of syringe will raise
usual automatically. The progress will signal by clear latching noises, 6 ‚clicks’ are a 360°-turn. (10)
11. Release mixing chamber from pressure by pushing the button and/or closing the stopcock. (11)
12. Remove filled injection device from stopcock by turning counter clockwise. (12)
13. Repeat procedure 9 to 12 as long as enough injection devices are filled or bone cement consumed totally.
US /
ENG
LISH

10/32
•Design dependent a small amount of cement mixture will remain in chamber and can not transferred. Usually the available
cement is sufficient.
•The already mixture should be transferred into an injection device or syringe as soon as possible, because of an increasing of
viscosity hampers aspiration. In dependence of cement behaviour there is a safe timeframe of 2-4 minutes.
•Per Click approx. 0,2 cc will be ejected dependently of consistency, viscosity and conditions.
5.3 Injection Systems and Injection
Cement Injection System (CIS
®
, Fig. 6) and Small Injection System (SIS, fig. 7)
1. Press the handles (4) together, submerge the nozzle (3) in the mixture, and draw in at least
3 ml of cement and push the whole volume back into the mixing bowl. In this manner, you will expel all air from the CIS® system.
When using the mixer system, the suction nozzle is not required and the injection system can be connected directly via the 2-way
stop cock (Fig. 4.7). Subsequently, follow the points 9-12 of this list of instructions in the chapter 5.2
2. Draw the whole desired volume into the CIS® system. In order to prevent suction of air bubbles, it is recommended that the
vessel be held at an angle with the nozzle (3) submerged into the cement mixture as deeply as possible.
3. The process of the filling of the device should take at least five seconds; too intense suction could cause the drawing in of air
bubbles. Accuracy of the scale in ml (1) is ±0,2 ml.
4. Remove the mandrin from the applicated cannula. The mandrin must remain sterile, because it will be used to push the remaining
cement from the inner cannula into the vertebral body.
5. Remove the nozzle (3) from the luer connector (2) of the CIS® system.
6. Attach the luer connector (2) of the CIS® system firmly to the cannula.
7. Wait until the cement is of a desired consistency.
8. Inject the cement with the assistance of radiological imaging. As soon as the cement can be applied only using a higher force, the
next step must commence. Otherwise, the cannula get fixed by hardened cement.
Beware: Using excessive force may mechanically damage the CIS® system.
9. Detach the luer connector (2) of the CIS® system from the cannula.
10. Place the mandrin back in the cannula and push the remaining cement in the cannula into the vertebral body. A table of residue
volumes of Somatex cannulas is available in the appropriate instructions for use.
11. During solidification of the cement, turn the cannula in specified time intervals (30-60 sec.) by 360° in order to prevent it becoming
fixed in the cement.
Workingtime of cement depends on injection device in accordance to graphs in pic. 6 and 7.
5.4. Aftercare
1. After complete hardening of cement withdrawal the canula through pulling and simultaneous turning of the canula. In
accordance with Fig. 2 a-f, the needle holder can be used to remove the cannula.
2. Take care for puncture point
6.Storage instructions and Disposal:
Storage instructions:
Store in a dark, dry place (humidity 30 – 65%) at a temperature between 41°F and 86° F (5°C – 30°C).
Disposal:
After using the product can be disposed in accordance to waste rules of hospitals.
US /
ENG
LISH

11/32
Mode d‘Utilisation (French)
Cet appareil a été préparé exclusivement pour une utilisation unique. Ce produit ne doit pas être utilisé une seconde fois après sa
première utilisation. Les qualités de la matière, les revêtements et les raccords collés peuvent être endommagés. Ce qui ne garantit
plus une application sûre du produit. Il n’a pas été conçu pour des processus de stérilisation et de nettoyage nécessaires après sa
première utilisation. De tels processus ne garantissent pas la stérilisation des produits à usage unique qui sont retraités. En
revanche, ils accroîssent considérablement le risque de blessures et d’infections accidentelles, en particulier des infections croisées
chez le patient et le personnel médical. L’entreprise Somatex décline toute responsabilité en cas de stérilisation et de réutilisation.
Ces instructions pour l’ensemble VERTEBROPLASTIE Somatex
®
n’a PAS pour but de définir ou de proposer des méthodes
médicales ou chirurgicales. Le médecin concerné est responsable du choix des procédures adaptées et des méthodes en rapport
avec ce produit.
1. Indication:
VERTEBROPLASTIE est utilisé pour la stabilisation du corps vertébral en utilisant du ciment osseux pour le traitement des fractures
pathologiques douloureuses par compression du corps vertébral qui ne peuvent pas être traitées par une intervention palliative
conventionnelle et qui sont marquées par:
- Ostéoporose primaire et secondaire
- Ostéolyses à partir de tumeurs dans la colonne vertébrale (carcinomes métastatiques ou myélomes),
- Ostéolyses des hémangiomes symptomatiques vertébraux.
Il doit être précisé que les procédures d’augmentation vertébrales sont uniquement des traitements palliatifs pour la stabilisation du
corps vertébral et des douleurs. Ils ne traitent pas les maladies causatives (ostéoporose ou tumeurs).
VERTEBROPLASTIE n’est pas adapté pour le traitement prophylactique des patients ostéoporotiques avec ou sans fractures du
corps vertébral.
2. Contre-indications
Ne pas appliquer VERTEBROPLASTIE lorsque le patient affiche une indication claire d’hypersensibilité aux composants de
l’ensemble et/ou au ciment osseux avec l’agent de contraste.
Contre-indications absolues:
- Grossesse ou allaitement
- Infections locales ou systémiques clarifiées de façon incomplète
- Maladies hémorragiques non contrôlables
Contre-indications relatives:
- Tumeurs du corps vertébral s’étendant à l’espace épidural
- Tumeurs vertébrales qui concernent le canal vertébral et qui occupent plus de 20% de la vertèbre
- Fractures par éclatement dans la colonne vertébrale
- Blessure anatomique du corps vertébral causée par un accès impropre au corps vertébral
- Manque de collaboration du ou des patient(s), qui n’est (ne sont) pas en position de suivre les instructions du personnel médical.
- Troubles du métabolisme qui interrompent la réaction de polymérisation du ciment osseux
- Ostéomalacie
- Infections générales qui peuvent potentiellement affecter le corps vertébral
- Hypotonie
- Insuffisance cardiaque
- Dysfonctionnement du rein
3. Description du produit _
(Image 1, fiche de couverture)
L’ensemble VERTEBROPLASTIE Somatex
®
est un produit stérile jetable qui est utilisé pour injecter du ciment osseux par une canule
dans le corps vertébral. Selon le modèle, il est composé d’une ou deux canules (1) pour des ponctions mono ou bilatérales, un
support d'aiguille (2) pour guider à l'extérieur de la canule vers le faisceau lumineux, un bol de mélange avec une spatule (4) ou un
système de mélange (3) et une ou deux petites seringues d’injection (SIS) (5) ou un système d’injection (CIS
®
) (6). Tous les
ensembles (Tableau 2) peuvent être complétés avec les accessoires spécifiés dans la liste (Tableau 3). 3).
4. Mises en garde
- La pression sanguine du patient sera étroitement surveillées pendant et juste après une vertébroplastie pour observer de
quelconques variations. Des réactions inverses au système cardiovasculaire du patient peuvent apparaître pendant l’application
des augmentations. Des réactions hypotoniques peuvent durer entre 5 secondes et plusieurs minutes après l’application du
ciment osseux. Dans de rares cas, elles peuvent mener à un arrêt cardiaque. Par conséquent, les patients doivent être
étroitement surveillés en ce qui concerne les fonctions vitales, juste après l’application du ciment osseux.
- Dans de rares cas, des effets secondaires sérieux, tels que l’infarctus myocardique, l’arrêt cardiaque, l’embolisme pulmonaire et
un AVC peuvent se produire dans le contexte d’une vertébroplastie.
- En cas de complication dans le système pulmonaire, cardiaque ou cardiovasculaire, il est nécessaire d’établir une condition
contrôlée et une volémie appropriée.
- Dans le cas d’une insuffisance respiratoire ou cardiaque aigüe ou d’une réanimation, le maintien des fonctions vitales doit être
assuré en utilisant des technologies appropriées.
- Avant l’implantation du ciment osseux, il est nécessaire d’exclure les risques ou les contre-indications. (Voir les contre-indications
absolues et relatives). En particulier, une inspection précise de la morphologie du corps vertébral cassé, d’une possible
vascularisation ou l’existence d’œdèmes devra être effectuée par des procédures d’imagerie adaptées.
- Avant d’effectuer une vertébroplastie, il convient de prendre des mesures de précaution pour corriger toutes complications par le
biais d’une intervention chirurgicale immédiate.
- La ponction d’un os avec la canule de vertébroplastie pourra être fait au moyen d’une procédure d’imagerie adaptée pour vérifier
le placement correct de la pointe de la canule.
- Il est obligatoire d’effectuer des augmentations vertébrales dans des conditions en temps réel sous illumination aux rayons x afin
de constater la distribution du ciment osseux dans l'expansion entière du corps vertébral et que l'utilisateur empêche la fuite du
ciment hors du corps vertébral.
- Un corps vertébral insuffisamment rempli ne peut pas corriger complètement les symptômes et peut signifier une stabilité
diminuée du corps vertébral traité.
FRENCH

12/32
- Dans le cas d’une fuite du ciment osseux hors du corps vertébral, les structures paravertébrales peuvent être endommagées, ce
qui signifie une compression possible de la moelle épinière, une douleur intercostale, une fuite dans l’espace intervertébral, un
remplissage des vaisseaux sanguins périvertébraux avec le risque d’embolie, d'infections et de douleurs post-opératoires.
- Une précaution sera exercée et les instructions du fabriquant suivie, tout en mélangeant le ciment osseux.
- Les instructions générales relatives au comportement et à la manipulation des instruments médicaux dans la zone stérile devront
être notées.
- Ne pas utiliser l’ensemble de VERTEBROPLASTIE SOMATEX
®
avec de quelconques composants, autres que ceux indiqués
dans la liste en tant qu’accessoires.
5. Application
5.1 Canule, Support d’aiguille et Préparation:
1. Avant l’utilisation, assurez-vous que l’emballage n’est pas ouvert et/ou endommagé; vérifiez la date de péremption et si la
dimension de la canule correspond ou pas à la spécification sur l’étiquette et que tous les composants sont disponibles.
2. La zone du dos à traiter devra être désinfectée pour marquer le corps vertébral et la zone devra être couverte de façon stérile.
3. Le cas échant, une incision devra être effectuée à la zone de ponction avec un scalpel afin de faciliter la pénétration dans la
peau.
4. La canule devra être reliée avec le support d’aiguille selon l’image 2 a-c. Elle est utilisée pour minimiser l’exposition aux
radiations de la main de l’opérateur aux radiations pendant la ponction. De plus, elle peut être utilisée pour un enlèvement facile
du mandrin (Image 2 d-f) ou similaire de la canule entière.
5. Placez la canule de vertébroplastie (Image 3) avec l'extrémité distale (1) et insérez soigneusement dans le tissu. Pendant la
visualisation sous l’illumination radiologique, poussez la canule en avant jusqu’à ce qu'il y est résistance du corps vertébral. Le
marquage (2) est utilisé pour l’orientation de la profondeur de pénétration.
6. Maintenant, fixez la canule soigneusement dans l’os ou par de petits coups de marteaux le cas échéant. Le support de l’aiguille
peut être retiré lorsque la canule a été fixée à sa place. Il convient de noter que le mandrin (4) est complètement logé dans la
connexion Luer Lock (3) et est bloqué pour éviter la rotation de la goupille. (5)
7. Vérifiez la position de la pointe de la canule (1) et l'angle correct par l'inspection CT/DSA et corrigez si nécessaire. Une encoche
de marquage sur le stylet (6) indique la position de la pointe de l’aiguille. Ceci facilitera l’orientation pour des corrections de
direction nécessaire.
8. Après l’alignement dans une position correcte, déplacez la canule plus loin dans le corps vertébral à l’aide de petits coups de
marteaux doux. En attendant, des inspections supplémentaires de position et/ou de direction seront effectuées avec l'imagerie
adaptée.
Diamètre de la canule en mm/G Longueur de la canule en mm Vol. interne en ml ** Canule de biopsie appropriée
3,00 / 11 100 0,45 2,0 / 14 x 150
3,00 / 11 125 0,55 2,0 / 14 x 200
3,00 / 11 150 0,65 2,0 / 14 x 200
2,50 / 12,5 125 0,31 -
2,00 / 14 125 0,24 -
Tab. 1 Dimensions de la canule
** Valeurs approximatives appliquées exclusivement aux canules de VERTEBROPLASTIE SOMATEX
Lorsque vous retirez une canule de vertébroplastie de la biopsie, faites attention aux dimensions correctes (Tab. de la canule de
biopsie et les instructions d’utilisation à suivre.
5.2 Préparation du ciment:
Les instructions du fabricant du ciment seront suivies, particulièrement les instructions de stockage et de température et les durées
de traitement. Selon le modèle, l’ensemble est équipé d’un système de mélange (Image 1.3) ou d’un bol de mélange avec une
spatule (Image 1.4).
a) Mélange avec le bol et la spatule
1. Mettre la poudre et le fluide du ciment osseux dans le bol. Assurez-vous que les deux sachets soient complètement vidés dans le
bol.
2. Mélangez les composants en utilisant la spatule pour former une masse homogène. Effectuez cette opération pendant 1 minute
pour obtenir une consistance uniforme.
b) Mélange avec le système de mélange (SOMIX 2.0), Images 4 et 5
REMPLISSAGE:
1. Dévissez le couvercle à vis du SOMIX
®
2.0 de la chambre en tournant dans le sens des aiguilles d’une montre. (1) Cette étape est
omise pour le kit ‘complet’.
2. Placez l’entonnoir sur la chambre de telle façon qu’il soit monté à même le centre. (2)
3. D’abords, remplissez la chambre avec la poudre puis avec le liquide. Assurez-vous que les quantités des composants soient
entièrement vidées et que rien ne soit renversé. (3) Plus tard, retirez une nouvelle fois l’entonnoir.
4. Fermez la chambre de mélange et vissez le couvercle à vis dans le sens horaire jusqu’à ce qu’un son clair se fasse entendre.
Les marquages appliqués sur la chambre affichent une fermeture correcte. (4)
MELANGE:
5. Vérifiez que le robinet est fermé. Déplacez la poignée inférieure rapidement par des mouvements poussez-tirez. Ceci fera bouger
la rame de haut en bas dans la chambre de mélange et assurera un mélange homogène et approfondi. Des rotations
supplémentaires de la poignée peuvent accélérer le processus de mélange (5).
Afin de garantir un mélange approfondi, il est recommandé de mener le processus de façon continue pendant au moins 30 à 40
secondes. La consistance sera contrôlée en visualisant la chambre de mélange transparente.
Si nécessaire, une aspiration peut-être appliquée par la connexion Luer Lock. Dans ce cas, le robinet sera resté ouvert.
FRENCH

13/32
TRANSFERT:
6. D’abords, ouvrez le robinet. Vissez la poignée inférieure dans le sens anti-horaire dans une condition complètement rétractée. (6)
Ceci aèrera la chambre.
7. Arrêtez le processus lorsque le palier de la chambre a atteint le début d’une étape et que le ciment remplit le robinet et le filtre. (7)
8. Retirez le filtre en dévissant dans le sens anti-horaire. (8)
9. Montez le système d’injection à remplir ou la seringue, de façon à ce qu’une connexion de joint serré est établie. (9)
10. Un vissage supplémentaire de la poignée inférieure transfère le ciment du système d’injection jusqu’à ce qu’il soit rempli. Le
piston du système d’injection se remonte lui-même normalement. L’avancement est signalé par des sons clairs, 6 clics pour une
rotation à 360°. (10)
11. Elevez la chambre de mélange de pression en appuyant sur le bouton et/ou fermez vers vous le robinet à 2 voies. (11)
12. Retirez le système d’injection du robinet en le tournant dans le sens anti-horaire. (12)
13. Répétez les étapes 9 à 12 jusqu’à ce que vous ayez suffisamment rempli les systèmes d’injection ou lorsque la chambre de
mélange est vide.
•Selon le concept, une petite quantité de mélange de ciment reste toujours dans la chambre et ne peut être transférée. En règle
générale, la quantité de ciment disponible est totalement suffisante.
•Après le mélange, le ciment sera transféré aussi rapidement que possible vers les seringues ou les systèmes d’injections car sa
viscosité croissante empêche son transfert. Selon les caractéristiques du ciment, son transfert dure 2 à 4 min.
•Selon la viscosité, la qualité et la consistance du ciment, environ 0,2ml est éjecté par clic.
5.3 Systèmes d’injection et Injection
Système d’injection du ciment (CIS
®
, Imag. 6) et système de petite injection (SIS, imag. 7)
1. Tirez la poignée (4) vers vous, maintenez le goulot d’aspiration (3) immergé dans le mélange, tirez au moins 3 ml de ciment et
faites ressortir toute la quantité dans le récipient utilisé pour le mélange. Ainsi, vous ferez sortir la totalité de l’air du Système
d’injection. Lorsque vous utilisez le système de mélange, l’embout d’aspiration n’est pas nécessaire et le système d’injection peut
être relié directement via le robinet à 2 voies (Imag. 4.7). Plus tard, suivez les points 9 à 12 de cette liste d’instructions dans le
chapitre 5.2.
2. A présent, aspirez dans le Système d’injection toute la quantité demandée de charge. Afin d’empêcher d’aspirer en même temps
des bulles d’air, nous vous recommandons de maintenir le récipient, après le mélange, incliné et d’immerger le goulot d’aspiration
aussi profond que possible dans le mélange du ciment.
3. Le processus d’aspiration du ciment devrait durer au minimum cinq secondes, dans la mesure où une aspiration trop intensive
peut faire de nouveau entrer des bulles d’air. La précision de l’échelle en ml (1=) est de ±0,2 ml.
4. Retirez attentivement la pointe intérieure de la canule placée. L’épine doit rester dans la région stérile, car c’est par son
intermédiaire que vous devrez repousser le ciment restant de la canule dans le corps de la vertèbre.
5. Enlevez le goulot d’aspiration (3) de la partie rotative (2) du système CIS®.
6. Vissez solidement la partie rotative (2) du système CIS® à la canule.
7. Attendez que le ciment atteigne la consistance demandée.
8. Injection du ciment à l’aide de l’imagerie radiologique. Au moment où il est encore possible d’appliquer le ciment mais en
employant un effort un peu plus important, vous devez immédiatement entamer la démarche suivante, sinon vous risquez de faire
durcir la canule.
Attention: l’emploi d’une force inadéquate peut avoir pour conséquence l’endommagement mécanique du Système
d’injection.
9. Dévissez la partie rotative (2) du système CIS
®
de la canule.
10. Introduisez de nouveau la pointe dans la canule et enfoncez le ciment restant à l’intérieur dans le corps de la vertèbre. Vous
trouverez le tableau des volumes résiduels dans les canules de l’entreprise Somatex pour la vertébroplastie dans le mode
d’emploi correspondant.
11. Pendant la phase de durcissement du ciment, tournez la canule dans certains intervalles réguliers (30 – 60 secondes) de 360°
afin d’empêcher le durcissement de l’aiguille dans le ciment.
Le temps de traitement du ciment doit être pris de façon dépendante du système d'injection et conformément aux diagrammes dans
fig. 6 et 7.
5.4 Suivi Médical
1. Après le durcissement du ciment, sortez l’aiguille par des mouvements rotatifs et en tirant du corps de la vertèbre. Selon l’image
2 a-f, le support de l’aiguille peut être utilisé pour retirer la canule.
2. Soignez l’endroit blessé.
6. Instructions de stockage et Elimination:
Instructions de stockage:
Stockez dans un lieu sur et sec (humidité 30 - 65 %) à une température entre 41°F et 86° F (5°C – 30 °C).
Elimination:
Après utilisation, le produit peut être éliminé selon la règlementation spécifique en matière d’élimination pour les déchets cliniques.
FRENCH

14/32
ΟΔΗΓΙΕΣ ΧΡΗΣΕΩΣ (Greek)
Το προϊό αυτό εί αι αποκλειστικά μίας χρήσεως. Απαγορεύεται ηεπα αχρησιμοποίηση του προϊό τος εφόσο χρησιμοποιηθεί μία
φορά. Ηποιότητα τω υλικώ , τω επιστρώσεω και τω κολλητώ συ δέσεω ε δέχεται α υποβαθμιστεί. Δε παρέχεται πλέο
καμία εγγύηση ασφαλούς χρήσης. Το προϊό δε εί αι σχεδιασμέ ο για τις απαιτούμε ες διαδικασίες καθαρισμού και αποστείρωσης
εφόσο χρησιμοποιηθεί μία φορά. Ως εκ τούτου δε παρέχεται καμία εγγύηση για τη στειρότητα προϊό τω μιας χρήσης τα οποία
υποβάλλο ται σε επα επεξεργασία. Οκί δυ ος ακούσιω βλαβώ και λοιμώξεω , ιδίως ετερολοιμώξεω μεταξύ ασθε ούς και
ιατρικού προσωπικού αυξά εται δυσα άλογα. Ηεταιρεία Somatex δε φέρει καμία ευθύ η σε περίπτωση επα αποστείρωσης και
επα άληψης της χρήσεως.
Οι παρούσες οδηγίες για τα σετ κο ιοπλαστικής σπο δύλω SOMATEX
®
ΔΕΝ αποσκοπού στο προσδιορισμό ήτη υπόδειξη
ιατρικώ ήχειρουργικώ μεθόδω . Τη ευθύ η για το προσδιορισμό τω κατάλληλω διαδικασιώ και μεθόδω όσο αφορά τη
εφαρμογή του παρό τος προϊό τος φέρει οαρμόδιος γιατρός.
1. Ενδείξεις:
ΗΚΟΝΙΟΠΛΑΣΤΙΚΗ ΣΠΟΝΔΥΛΩΝ χρησιμοποιείται ως μέθοδος σταθεροποίησης της δομής τω σπο δύλω με κο ίαμα οστώ , για
τη α τιμετώπιση επώδυ ω , παθολογικής αιτιολογίας συμπιεστικώ καταγμάτω , τα οποία δε μπορού α α τιμετωπιστού με
συ τηρητική α αλγητική θεραπεία και έχου τα εξής χαρακτηριστικά:
- πρωτογε ής και δευτερογε ής οστεοπόρωση,
- οστεόλυση λόγω όγκω στο σώμα του σπο δύλου (μεταστατικά καρκι ώματα ήμυελώματα),
- οστεόλυση λόγω συμπτωματικώ αιμαγγειωμάτω σπο δύλω .
Να σημειωθεί ότι ηε ίσχυση τω σπο δύλω αποτελεί απλά παρηγορητική αγωγή για τη σταθεροποίηση του σώματος τω
σπο δύλω και τη α ακούφιση του άλγους. Δε α τιμετωπίζει το γε εσιουργό όσημα (οστεοπόρωση ήεοπλασία).
ΗΚΟΝΙΟΠΛΑΣΤΙΚΗ ΣΠΟΝΔΥΛΩΝ δε ε δείκ υται ως προληπτική θεραπεία κατά της οστεοπόρωσης με ήχωρίς κατάγματα
σπο δύλω .
2. Αντενδείξεις
Μη εφαρμόζετε ΚΟΝΙΟΠΛΑΣΤΙΚΗ ΣΠΟΝΔΥΛΩΝ ότα υφίσταται γ ωστή υπερευαισθησία του ασθε ούς στα συστατικά του σετ και/ή
στο κο ίαμα οστώ με σκιαστική ουσία.
Απόλυτες αντενδείξεις:
- εγκυμοσύ η ήθηλασμός
- μη επαρκώς διερευ ηθείσες τοπικές ήσυστημικές λοιμώξεις
- μη ελεγχόμε α αιμορραγικά οσήματα
Σχετικές αντενδείξεις:
- σπο δυλικοί όγκοι με επισκληρίδιο διείσδυση
- σπο δυλικοί όγκοι που εκτεί ο ται στο σπο δυλικό σωλή α και καταλαμβά ου περισσότερο από το 20% του σπο δύλου
- συμπιεστικά κατάγματα στο εσωτερικό της σπο δυλικής στήλης
- α ατομικές βλάβες στο σώμα τω σπο δύλω λόγω της μη ασφαλούς πρόσβασης στο σπό δυλο
- μη συ εργασία του ασθε ούς ήασθε ής που δε εί αι σε θέση α ακολουθήσει τις οδηγίες του ιατρικού προσωπικού
- μεταβολικά οσήματα με επίδραση στη α τίδραση πολυμερισμού του κο ιάματος οστώ
- οστεομαλάκυ ση
- μη τοπικές λοιμώξεις, οι οποίες δύ α ται α πλήξου το σπό δυλο
- υπόταση
- καρδιακή α επάρκεια
- εφρική α επάρκεια
3. Περιγραφή προϊόντος
(εικ.1, εξώφυλλο)
Το σετ ΚΟΝΙΟΠΛΑΣΤΙΚΗΣ ΣΠΟΝΔΥΛΩΝ Somatex
®
εί αι έ α αποστειρωμέ ο προϊό μιας χρήσεως, που χρησιμοποιείται για τη
έγχυση κο ιάματος οστώ στο σώμα του σπο δύλου μέσω μιας βελό ης. Α άλογα με τη παραλλαγή, αποτελείται από μία ήδύο
βελό ες (1) μο ής ήδιπλής παρακέ τησης, έ α βελο οκάτοχο (2) για το χειρισμό της βελό ης εκτός του πεδίου ακτι οβολίας, έ α
δοχείο α άμειξης με α αδευτήρα (4) ήέ α σύστημα α άμειξης (3) και μία ήδύο μικρές σύριγγες (SIS) (5) ήέ α σύστημα έγχυσης
(CIS
®
) (6). Όλα τα σετ (πί . 2) μπορού α συμπληρωθού με τα εξαρτήματα που περιλαμβά ο ται στη λίστα (πί . 3).
4. Προειδοποιήσεις
- Κατά τη διάρκεια της κο ιοπλαστικής σπο δύλου α παρακολουθείται προσεκτικά ηαρτηριακή πίεση του ασθε ούς για τυχό
μεταβολές. Κατά τη εφαρμογή ε ισχύσεω ε δέχεται α παρατηρηθού α επιθύμητες α τιδράσεις του καρδιαγγειακού
συστήματος του ασθε ούς. Ηπτώση της πίεσης μπορεί α διαρκέσει από 5 δευτερόλεπτα έως και αρκετά λεπτά μετά τη
εφαρμογή του κο ιάματος οστώ . Σε σπά ιες περιπτώσεις μπορεί α προκληθεί καρδιακή α ακοπή. Γι' αυτό επιβάλλεται η
προσεκτική παρακολούθηση τω ζωτικώ λειτουργιώ του ασθε ούς κατά το διάστημα που ακολουθεί τη εφαρμογή του
κο ιάματος.
- Σε σπά ιες περιπτώσεις, μετά τη κο ιοπλαστική σπο δύλου δε αποκλείο ται σοβαρές παρε έργειες, όπως έμφραγμα του
μυοκαρδίου, καρδιακή α ακοπή, εγκεφαλικό επεισόδιο και π ευμο ική εμβολή.
- Σε περίπτωση επιπλοκώ στους π εύμο ες ήτο καρδιαγγειακό σύστημα επιβάλλεται ηα άκτηση του ελέγχου του οργα ισμού
και της αιμάτωσης.
- Σε περίπτωση οξείας α απ ευστικής ήκαρδιακής α επάρκειας ήα ά ηψης θα πρέπει α αποκατασταθού με τις ε δεδειγμέ ες
μεθόδους οι ζωτικές λειτουργίες του ασθε ούς.
- Πρι τη εμφύτευση του κο ιάματος οστώ εί αι α αγκαίος οαποκλεισμός πιθα ώ κι δύ ω ήα τε δείξεω . (βλ. επίσης
απόλυτες και σχετικές α τε δείξεις). Ιδιαίτερα σημα τικό εί αι α διε εργηθεί ε δελεχής έλεγχος της μορφολογίας του σώματος
σπο δύλου που έχει σπάσει και α ε τοπιστού ε δεχόμε ες αγγειοποιήσεις ήοιδήματα με χρήση της κατάλληλης απεικο ιστικής
μεθόδου.
- Πρι τη κο ιοπλαστική σπο δύλου πρέπει α ληφθού προληπτικά μέτρα για τη άμεση επεμβατική α τιμετώπιση ε δεχόμε ω
επιπλοκώ .
- Ηπαρακέ τηση του οστού με τη βελό η κο ιοπλαστικής σπο δύλου πρέπει α πραγματοποιηθεί με χρήση μιας κατάλληλης
απεικο ιστικής μεθόδου, προκειμέ ου α εξασφαλιστεί ηορθή τοποθέτηση της βελό ης.
GREEK

15/32
- Ηεφαρμογή σπο δυλικώ ε ισχύσεω πρέπει α εκτελείται οπωσδήποτε υπό ακτι οσκοπική παρακολούθηση πραγματικού
χρό ου, προκειμέ ου α εί αι ορατή ηδια ομή του κο ιάματος σε ολόκληρη τη έκταση του σπο δύλου και α αποφευχθεί η
διαρροή του κο ιάματος εκτός του σπο δύλου.
- Ηα επαρκής πλήρωση του σπο δύλου μπορεί α έχει ως συ έπεια τη μη ικα οποιητική υπό ορισμέ ες συ θήκες α τιμετώπιση
τω συμπτωμάτω και τη μακροπρόθεσμη αστάθεια του σπο δύλου.
- Σε περίπτωση διαρροής του κο ιάματος εκτός του σπο δύλου, ε δέχεται α προκληθού βλάβες στις παρασπο δυλικές δομές,
συμπίεση του ωτιαίου μυελού, μεσοπλευρικά άλγη, διαρροές στο μεσοσπο δύλιο χώρο, πλήρωση τω περισπο δυλικώ
αιμοφόρω αγγείω με κί δυ ο εμβολής, μολύ σεις και μετεγχειρητικά άλγη.
- Κατά τη διάρκεια της α άμειξης του κο ιάματος συ ιστάται προσοχή και αυστηρή εφαρμογή τω οδηγιώ του κατασκευαστή.
- Να λαμβά ο ται υπόψη οι γε ικοί κα ο ισμοί, οι οποίοι διέπου τη συμπεριφορά και τη χρήση ιατρικώ εργαλείω σε
αποστειρωμέ ο περιβάλλο .
- Μη συ δυάζετε το σετ κο ιοπλαστικής σπο δύλου SOMATEX
®
με άλλα εξαρτήματα, που δε συμπεριλαμβά ο ται στη λίστα
εξαρτημάτω .
5. Εφαρμογή
5.1 Βελόνη, βελονοκ τοχο και προετοιμασία:
1. Πρι τη χρήση, βεβαιωθείτε ότι ησυσκευασία δε εί αι α οιγμέ η και/ήαλλοιωμέ η. Ελέγξτε τη ημερομη ία αποστείρωσης,
συγκρί ετε το μέγεθος της βελό ης με τα στοιχεία της ετικέτας και βεβαιωθείτε ότι υπάρχου όλα τα εξαρτήματα.
2. Αποστειρώστε το σχετικό τμήμα της ράχης, σημειώστε το σπό δυλο και καλύψτε τη περιοχή με αποστειρωμέ ο υλικό.
3. Εά εί αι σκόπιμο, α οίξτε μια τομή στο σημείο παρακέ τησης με έ α υστέρι, προκειμέ ου α διευκολύ ετε τη είσοδο στο
δέρμα.
4. Συ δέστε τη βελό η με το βελο οκάτοχο σύμφω α με τη εικ. 2 a-c. Το βελο οκάτοχο προστατεύει το χέρι του χειρουργού από
τη ακτι οβολία κατά τη παρακέ τηση. Επιπλέο , μπορεί α βοηθήσει στη ευκολότερη αφαίρεση του σύρματος-οδηγού (εικ. 2
d-f) ήα τιστοίχως ολόκληρης της βελό ης.
5. Πιάστε τη βελό η κο ιοπλαστικής σπο δύλω (εικ. 3) από το έ α άκρο (1) και εισαγάγετέ τη προσεκτικά στο ιστό. Ωθήστε τη
υπό ακτι οσκοπικό έλεγχο, έως ότου ιώσετε τη α τίσταση του σπο δύλου. Το σημάδι (2) σας βοηθά α προσδιορίσετε το
βάθος διείσδυσης.
6. Τώρα στερεώστε προσεκτικά τη βελό η μέσα στο οστό, ε δεχομέ ως χτυπώ τας τη ελαφρά με έ α σφυρί. Ότα σταθεροποιηθεί
ηθέση της βελό ης, μπορείτε α απομακρύ ετε το βελο οκάτοχο. Λάβετε υπόψη ότι ολόκληρο το σύρμα-οδηγός (4) πρέπει α
βρίσκεται μέσα στη σύ δεση Luer (3) και α εί αι ασφαλισμέ ο με το πείρο (5), ώστε α μη μπορεί α μετατοπιστεί.
7. Ελέγξτε τη θέση της μύτης (1) και τη γω ία της βελό ης με CT/DSA και κά τε τις α αγκαίες διορθώσεις. Οι εγχάρακτες ε δείξεις
στη βάση του στιλέτου (6) υποδηλώ ου τη θέση της μύτης της βελό ης. Με αυτό το τρόπο διευκολύ ου το προσα ατολισμό
του χειρουργού για τις α αγκαίες διορθώσεις κατεύθυ σης.
8. Μετά τη διόρθωση της θέσης, ωθήστε τη βελό η πιο βαθειά στο σώμα του σπο δύλου με ελαφρά και στοχευμέ α χτυπήματα. Ε
τω μεταξύ θα πρέπει α διε εργού ται συ εχείς έλεγχοι της θέσης και/ήτης κατεύθυ σης με τη κατάλληλη απεικο ιστική μέθοδο.
διατομή βελό ης σε mm/G μήκος βελό ης σε mm εσ. χωρητικότητα σε ml ** κατάλληλη βελό η βιοψίας
3,00 / 11 100 0,45 2,0 / 14 x 150
3,00 / 11 125 0,55 2,0 / 14 x 200
3,00 / 11 150 0,65 2,0 / 14 x 200
2,50 / 12,5 125 0,31 -
2,00 / 14 125 0,24 -
Πίν.1, Διαστάσεις βελό ης
** οι κατά προσέγγιση τιμές ισχύου αποκλειστικά για βελό ες κο ιοπλαστικής SOMATEX
Σε περίπτωση λήψη δείγματος για βιοψία μέσω της βελό ης κο ιοπλαστικής α επιλέγο ται οι σωστές διαστάσεις (πί . 1) της βελό ης
βιοψίας και α ακολουθού ται οι οδηγίες χρήσεως.
5.2 Προετοιμασία του κονι ματος:
Να εφαρμόζο ται οι οδηγίες του κατασκευαστή του κο ιάματος, ιδιαίτερα όσο αφορά τις υποδείξεις φύλαξης και θερμοκρασίας ή
τους χρό ους παρασκευής. Α άλογα με τη παραλλαγή, το σετ περιλαμβά ει έ α σύστημα α άμειξης (εικ.1.3) ήέ α δοχείο α άμειξης
με α αδευτήρα (εικ. 1.4).
α) Αν μειξη με δοχείο και αναδευτήρα
1. Γεμίστε το δοχείο με τη σκό η και το υγρό του κο ιάματος οστώ . Φρο τίστε α μεταφέρετε στο δοχείο ολόκληρη τη ποσότητα
που περιέχεται στις δύο συσκευασίες χωρίς απώλειες.
2. Α αμείξτε τα συστατικά με τη βοήθεια του α αδευτήρα, έως ότου γί ου μια ομοιογε ής μάζα. Αυτή ηδιαδικασία πρέπει α
διαρκέσει περ. 1 λεπτό χωρίς διακοπή, ώστε α δημιουργηθεί έ α μείγμα με ε ιαία υφή.
β) Αν μειξη με σύστημα αν μειξης (SOMIX 2.0), εικ. 4 και 5
ΠΛΗΡΩΣΗ:
1. Περιστρέψτε το πώμα του SOMIX
®
2.0 προς τα αριστερά και αφαιρέστε το από το θάλαμο. (1) Αυτό το βήμα δε ισχύει για το σετ
"complete".
2. Τοποθετήστε τη χοά η πά ω στο θάλαμο, έτσι ώστε α εί αι ευθυγραμμισμέ η και κε τραρισμέ η σωστά. (2)
3. Πρώτα γεμίστε το θάλαμο με τη σκό η κι έπειτα με το υγρό. Φρο τίστε α χρησιμοποιήσετε ολόκληρη τη ποσότητα τω δύο
συστατικώ και α μη χυθεί τίποτα έξω. (3) Έπειτα αφαιρέστε ξα ά τη χοά η.
4. Κλείστε το θάλαμο α άμειξης βιδώ ο τας το πώμα με δεξιόστροφες κι ήσεις, έως ότου το ιώσετε α ασφαλίζει καλά. Τα σημάδια
πά ω στο θάλαμο σάς δείχ ου εά το σφράγισμα έχει πραγματοποιηθεί σωστά. (4)
GREEK

16/32
ΑΝΑΜΕΙΞΗ:
5. Ελέγξτε εά εί αι κλειστή ηστρόφιγγα. Αρχίστε α σπρώχ ετε και α τραβάτε με γρήγορο ρυθμό τη λαβή. Οα αδευτήρας του
θαλάμου α άμειξης κι είται πά ω κάτω και φρο τίζει για τη ομοιόμορφη α άμειξη του υλικού. Πρόσθετες περιστροφικές κι ήσεις
της λαβής μπορού α επιταχύ ου τη διαδικασία α άμειξης (5).
Για α εξασφαλιστεί ηπλήρης α άμειξη, συ ιστάται α συ εχίσετε τη διαδικασία χωρίς διακοπή για τουλ. 30-40 sec. Η
ομοιογέ εια του υλικού πρέπει α ελεγχθεί στο διαφα ή θάλαμο α άμειξης.
Εά εί αι α αγκαίο, μπορεί α συ δεθεί έ α σύστημα υποπίεσης μέσω της σύ δεσης Luer. Στη περίπτωση αυτή πρέπει α
α οίξετε τη στρόφιγγα.
ΜΕΤΑΦΟΡΑ
6. Κατ' αρχάς α οίξτε τη στρόφιγγα. Βιδώστε τη κάτω λαβή σε ε τελώς κλειστή κατάσταση περιστρέφο τάς τη προς τα αριστερά.
(6) Έτσι αποβάλλεται οαέρας από το θάλαμο.
7. Σταματήστε τη διαδικασία ότα οπυθμέ ας του θαλάμου φθάσει στη κλίμακα και το κο ίαμα έχει γεμίζει τη στρόφιγγα και το
φίλτρο. (7)
8. Αφαιρέστε το φίλτρο ξεβιδώ ο τάς το αριστερόστροφα. (8)
9. Τοποθετήστε το σύστημα έγχυσης ήτη σύριγγα που θέλετε α γεμίσετε, φρο τίζο τας α εί αι στεγα ή ησύ δεση. (9)
10. Το κο ίαμα μεταφέρεται στο σύστημα έγχυσης με περιστροφή της κάτω λαβής, ώσπου α γεμίσει το σύστημα. Κα ο ικά, το
έμβολο του συστήματος έγχυσης σηκώ εται από μό ο του. Ηπρόοδος σηματοδοτείται με διακριτούς ήχους ασφάλισης, όπου 6
"κλικ" ισοδυ αμού με μία περιστροφή 360°. (10)
11. Εκτο ώστε τη πίεση στο θάλαμο α άμειξης πιέζο τας το κουμπί και/ήκλεί ο τας τη δίοδη στρόφιγγα. (11)
12. Αφαιρέστε το σύστημα έγχυσης από τη στρόφιγγα περιστρέφο τάς προς τα αριστερά. (12)
13. Επα αλάβετε τα βήματα 9 έως 12, έως ότου γεμίσετε αρκετά συστήματα έγχυσης ήαδειάσει οθάλαμος α άμειξης.
•Για κατασκευαστικούς λόγους, στο θάλαμο παραμέ ει μια ελάχιστη ποσότητα μείγματος που δε μπορεί α απομακρυ θεί. Κατά
κα ό α, ηδιαθέσιμη ποσότητα κο ιάματος εί αι απόλυτα επαρκής.
•Το κο ίαμα πρέπει α μεταφερθεί σε σύριγγες ήσυστήματα έγχυσης το συ τομότερο δυ ατό μετά τη α άμειξη, επειδή το
αυξα όμε ο ιξώδες δυσχεραί ει τη μεταφορά. Σε συ άρτηση με τη συμπεριφορά του κο ιάματος, το διαθέσιμο χρο ικό διάστημα
για τη μεταφορά εί αι 2-4 min.
•Α άλογα με το ιξώδες, τη ποιότητα και τη σύσταση του κο ιάματος εκτι άσσο ται α ά κλικ περ. 0,2 ml.
5.3 Συστήματα έγχυσης και έγχυση
Cement Injection System (CIS
®
, εικ. 6) και Small Injection System (SIS, εικ. 7)
1. Πιέστε τη λαβή(4), κρατήστε το ρύγχο (3) μέσα στο μείγμα της συ δετικής ύλης και αφήστε α α αρροφηθού το λιγότερο 3ml
συ δετικής ύλης και επα ατοποθετήστε τη όλη στο δοχείο προπαρασκευής. Με τη κί ηση αυτή θα επιτευχθεί ηαποβολή όλου
του αέρα από το Συστήματα έγχυσης. Στη περίπτωση του συστήματος α άμειξης δε απαιτείται ηχρήση του στομίου
α αρρόφησης και το σύστημα έγχυσης συ δέεται απευθείας με τη δίοδη στρόφιγγα (εικ. 4.7). Στη συ έχεια, ακολουθήστε τα
σημεία 9-12 στο κεφάλαιο 6.2 τω οδηγιώ αυτώ .
2. Εισάγετε μό ο τη επιθυμητή ποσότητα στο Συστήματα έγχυσης. Για α αποφευχθεί ηδημιουργία φυσαλιδώ αέρος μέσα στο
Συστήματα έγχυσης ε δείκ υται ητοποθέτηση του δοχείου προπαρασκευής υπό γω ία και ηόσο το δυ ατό μεγαλύτερη βύθιση
του ρύγχου στη στείρα συ δετική ύλη.
3. Ηδιαδικασία α αρρόφησης πρέπει α διαρκέσει το λιγότερο πέ τε δευτερόλεπτα, καθότι θα μπορούσα και πάλι α
δημιουργηθού φυσαλίδες αέρος μέσω ε ός δυ ατού ρεύματος. Ηακρίβεια της κλίμακας ml(1) κυμαί εται στο
±0,2 ml.
4. Απομακρύ ετε προσεκτικά το οδηγό σύρμα από τη τοποθετημέ η βελό η. Οοδηγός σύρμα πρέπει α παραμεί ει σε
αποστειρωμέ ο χώρο, καθότι με αυτό πρέπει α εισαχθεί ηυπόλοιπη συ δετική ύλη από τη βελό η στη σπο δυλική στήλη.
5. Απομακρύ ετε το ρύγχο(3) από το περιστροφέα (2) του CIS®.
6. Βιδώστε σφιχτά το περιστροφέα(2) του Συστήματα έγχυσης πά ω στη βελό η.
7. Περιμέ ετε έως ότου ησυ δετική ύλη αποκτήσει τη επιθυμητή πυκ ότητα.
8. Ε δοφλέβια έγχυση συ δετικής ύλης υπό ραδιολογική παρακολούθηση. Σε αυτό το σημείο θα πρέπει α δοθεί ιδιαίτερη προσοχή
στη χρο ική διάρκεια της πήξης της συ δετικής ύλης. Μο άχα ότα καταστεί δυ ατή ηχορήγηση της συ δετικής ύλης με ακόμη
περισσότερη πίεση, θα πρέπει α προχωρήσετε στο επόμε ο βήμα, γιατί υπάρχει οκί δυ ος τσιμε τοποίησης της βελό ης.
Προσοχή: Ηυπερβολική πίεση μπορεί να οδηγήσει σε μηχανικές βλ βες του Συστήματα έγχυσης.
9. Ξεβιδώστε το περιστροφέα (2) του Συστήματα έγχυσης από τη βελό η.
10. Τοποθετήστε το οδηγό σύρμα πάλι στη βελό η και εισάγετε τη υπόλοιπη συ δετική ύλη από τη βελό η στη σπο δυλική στήλη.
Πί ακες του υπόλοιπου όγκου της συ δετικής ύλης μπορού α βρεθού στις οδηγίες χρήσεως τω βελό ω
σπο δυλοπλαστικής Somatex.
11. Κατά τη διάρκεια πήξης της συ δετικής ύλης πρέπει α περιστραφού οι βελό ες κατά 360° επα ειλλημέ α σε συγκεκριμέ α
χρο ικά διαστήματα (30-60 δευτερόλεπτα) για α αποφευχθεί ητσιμε τοποίηση της βελό ης.
Οχρό ος απασχόλησης του τσιμέ του εξαρτάται από τη συσκευή εγχύσεω σύμφω α με τις γραφικές παραστάσεις στη εικό α. 6
και 7.
5.4. παρακολούθηση
1. Μετά τη πήξη της συ δετικής ύλης απομακρύ ετε τη βελό η με το χέρι από τη σπο δυλική στήλη περιστροφικά ήτραβώ τας
τη . Όπως φαί εται στη εικ.2 a-f, για τη αφαίρεση της βελό ης μπορεί α χρησιμοποιηθεί το βελο οκάτοχο
2. Φρο τίστε τη πληγή.
6. Οδηγίες φύλαξης και Απόρριψη:
Οδηγίες φύλαξης:
Φύλαξη σε σκοτει ό, ξηρό χώρο (ατμοσφαιρική υγρασία 30% - 65%) με θερμοκρασία 41°F - 86° F (5°C – 30°C).
Απόρριψη:
Το προϊό μπορεί α απορριφθεί μετά τη χρήση σύμφω α με τους κα ο ισμούς διάθεσης οσοκομειακώ αποβλήτω .
GREEK

17/32
Istruzioni per l’uso (Italian)
Questo strumento è stato prodotto esclusivamente per il monouso. Il prodotto monouso non può essere riutilizzato, perché la qualità
dei materiali, i rivestimenti e le giunzioni incollate possono risultarne compromessi. Non è più garantito un impiego sicuro. Il prodotto
monouso non è stato realizzato per essere sottoposto ai processi di pulizia e di sterilizzazione necessari. Pertanto, non è garantita la
sterilità dei prodotti monouso ritrattati. Il rischio di ferite e infezioni involontarie, soprattutto di infezioni crociate, del paziente e del
personale medico aumenta in modo rilevante. La ditta Somatex declina da qualsiasi responsabilità nel caso della sterilizzazione
ripetuta e dell’uso ripetuto dello strumento.
Le presenti istruzioni per il set di vertebroplastica SOMATEX
®
NON hanno lo scopo di proporre o dettare metodi medico-chirurgici. Il
medico interessato è responsabile dell'adozione delle appropriate procedure e metodi associati all'uso di questo prodotto.
1. Indicazioni cliniche:
La VERTEBROPLASTICA serve a stabilizzare la struttura del corpo vertebrale con cemento osseo nel trattamento di fratture da
cedimento del corpo vertebrale, patologiche, sintomatiche, refrattarie alla terapia antalgica e causate da:
- osteoporosi primaria o secondaria;
- osteolisi da lesioni neoplastiche primarie o secondari (mielomi o metastasi ossee);
- osteolisi da lesioni tumorali benigne (emangiomi vertebrali sintomatici).
Va tenuto presente che la vertebroplastica e la cifoplastica percutanea sono solo trattamenti palliativi volti ad ottenere la riduzione del
dolore provocato dal cedimento vertebrale mediante stabilizzazione e rinforzo del corpo vertebrale danneggiato. Esse si affiancano,
ma non sostituiscono le procedure terapeutiche necessarie a curare la patologia di base (osteoporosi o malattie tumorali).
Non è previsto l’uso di VERTEBROPLASTICA come profilassi in soggetti osteopenici in assenza di fratture accertate a carico delle
vertebre da trattare.
2. Controindicazioni
Non usare VERTEBROPLASTICA in casi di accertata ipersensibilità ai componenti del set e/o del cemento con mezzo di contrasto.
Controindicazioni assolute:
- lo stato di gravidanza o l’allattamento;
- le infezioni locali o sistemiche in atto o non completamente trattate;
- le coagulopatie non correggibili.
Controindicazioni relative:
- lesioni neoplastiche del corpo vertebrale con estensione allo spazio epidurale;
- lesioni neoplastiche con invasione del canale vertebrale (occlusione maggiore del 20%);
- presenza di un frammento osseo espulso posteriormente e causa di mielopatia;
- danno anatomico delle vertebre che pregiudichi un sicuro accesso dell’ago nel corpo vertebrale.
- paziente non collaborativo o con disordini neurologici che non lo rendono in grado di seguire le indicazioni da parte
dell’operatore;
- patologie metaboliche che alterino la formazione del cemento osseo;
- osteomalacia;
- foci di infezione distanti che tuttavia potrebbero interessare la zona di impianto;
- ipotensione;
- sindrome cardiaca congestizia;
- insufficienza renale.
3. Descrizione del prodotto
(Fig.1, Copertina)
Il set per vertebroplastica Somatex® è un prodotto usa e getta che serve all’iniezione di cemento osseo attraverso una cannula nel
corpo vertebrale. A seconda della variante essa è costituita da una o due cannule (1) per puntura mono o bilaterale, un supporto per
ago (2) per la guida delle cannule attraverso il percorso, un recipiente di miscelazione con spatola (4) o un sistema di miscelazione
(3) e una o due cannule piccole per iniezione (SIS) (5) o un sistema di iniezione (CIS
®
) (6). Tutti i set (Tab. 2) possono essere
completati con gli accessori specifici (Tab. 3) riportati nella lista.
4. Avvertenze e precauzioni
- Controllare la pressione sistolica del paziente in modo sistematico ed accurato durante e dopo l’applicazione del cemento. In
letteratura sono state osservate reazioni individuali che interessano il sistema cardiovascolare che sono state correlate in
generale all’uso di cementi ossei. In questi casi si sono verificati episodi ipotensivi in un periodo compreso tra 5 secondi e più
minuti dall’impianto. Sono stati riportati rari casi di arresto cardiaco. Dopo l’applicazione del cemento osseo le funzioni vitali del
paziente devono essere monitorate con attenzione.
- In casi rari in relazione alla vertebroplastica sono stati riscontrati gravi effetti collaterali come infarto, arresto cardiaco, ictus ed
embolia polmonare.
- In caso di complicazioni cardiovascolari o polmonari si rende necessario procedere ad un controllo ed eventualmente ad un
ripristino della volemia.
- In caso di insufficienza respiratoria acuta o di arresto cardiaco ricorrere alle specifiche tecniche di rianimazione per il ripristino
delle funzioni vitali.
- In fase pre-operatoria deve essere effettuata un’indagine sul paziente per escludere eventuali situazioni di rischio o l’esistenza di
condizioni che escludono l’esecuzione della procedura. (vedi controindicazioni assolute e relative). In particolare deve essere
effettuato un accurato controllo radiografico delle condizioni morfologiche della lesione del corpo vertebrale, della eventuale
intervenuta vascolarizzazione del corpo vertebrale leso o presenza di edema.
- Prima di applicare il cemento, come misura cautelativa, deve essere prevista la possibilità di un intervento operatorio immediato
per rimediare chirurgicamente alle complicazioni della procedura percutanea.
- La puntura dell’osso con cannule per vertebroplastica deve essere effettuata con l'ausilio delle appropriate procedure illustrate,
per verificare la corretta posizione della punta della cannula.
- L’applicazione deve essere effettuata necessariamente con procedura guidata per immagini adeguata a controllare il riempimento
e la distribuzione del cemento nel corpo vertebrale in tutta la sua estensione spaziale ed evitarne la fuoriuscita.
- Un riempimento incompleto del corpo vertebrale porta ad una possibile riduzione insufficiente dei sintomi e ad una stabilità ridotta
nel tempo del corpo vertebrale trattato.
ITALIAN

18/32
- In caso di fuoriuscita del cemento dal corpo vertebrale possono venir danneggiate le strutture paravertebrali ed intervenire
complicazioni quali compressione del midollo spinale, nevralgia intercostale, fuoriuscita del cemento nello spazio intervertebrale,
riempimento perivertebrale delle vene e delle arterie (rischio d’embolia), infezioni e dolori post operatori.
- Usare cautela durante la fase di mescolamento seguendo scrupolosamente le istruzioni.
- Attenersi alle prescrizioni generali relative all'utilizzo di strumentazioni mediche in campo sterile.
- Non è possibile combinare il set per vertebroplastica SOMATEX
®
con nessun altro componente diverso da quelli riportati
nell’elenco come accessori.
6. Applicazione
6.1 Cannula, supporto per ago e preparazione:
1. Prima dell'uso, accertarsi che la confezione non sia aperta e/o danneggiata, verificare la data di sterilizzazione, controllare che la
grandezza della cannula corrisponda a quella riportata sull’etichetta e che tutti i componenti siano presenti.
2. Disinfettare la parte di schiena da trattare, contrassegnare il corpo vertebrale e coprire l'area sterile.
3. Event. effettuare un’incisione sul punto di iniezione con un bisturi, per facilitare la penetrazione della pelle.
4. Collegare la cannula con il supporto ago come mostrato nella Fig. 2 a-c. Esso serve per la riduzione dell’esposizione alle
radiazioni della mano dell’operatore durante la puntura. Inoltre esso può essere utilizzato per la rimozione semplice del mandrino
(Fig. 2 d-f) o analoga cannula disponibile.
5. Posizionare la cannula per vertebroplastica (Fig. 3) con l'estremità distale e inserire con attenzione nel tessuto. Sotto visione
radiologica spingere in avanti la cannula, finché diventa percepibile la resistenza attraverso il contatto con il corpo vertebrale. La
marcatura (2) serve per l’orientamento della profondità di penetrazione.
6. Ora fissare la cannula con attenzione all’osso, se serve con leggeri colpi di martello. Quando la cannula è posizionata in modo
sicuro, è possibile rimuovere il supporto dell'ago. Fare attenzione che il mandrino (4) sia completamente nel raccordo Luer (3) e
assicurato con il perno (5) per evitare che ruoti.
7. Verificare la posizione della punta della cannula (1) e la corretta angolazione mediante controllo CT/DSA e se è il caso
correggere. Una marcatura sulla parte iniziale dello stiletto (6) mostra la posizione della punta dell’ago. In caso di necessità della
correzione della direzione, ciò può facilitare l’orientamento.
8. Dopo l’allineamento in posizione corretta spingere nuovamente la cannula nel corpo vertebrale con leggeri e mirati colpi di
martello. Intanto effettuare ulteriori controllo della posizione e della direzione mediante immagini adeguate.
Diametro cannula in mm/G Lunghezza cannula in mm
Volume interno in ml ** Cannula per biopsia
3,00 / 11 100 0,45 2,0 / 14 x 150
3,00 / 11 125 0,55 2,0 / 14 x 200
3,00 / 11 150 0,65 2,0 / 14 x 200
2,50 / 12,5 125 0,31 -
2,00 / 14 125 0,24 -
Tab.1, Dimensioni cannula
** i valori valgono per cannule per vertebroplastica SOMATEX
In caso di biopsia osservare se la cannula per vertebroplastica sia delle dimensioni corrette (Tab. 1) per la cannula per biopsia e
seguire le istruzioni per l’uso.
5.2 Preparazione del cemento:
Osservare le istruzioni del produttore di cemento, in particolare le indicazioni relative alla temperatura e alla conservazione, e il tempo
di lavorazione. A seconda della variante il set è dotato di sistema di miscelazione (Fig. 1.3) o un recipiente di miscelazione con
spatola (Fig. 1.4).
a) Miscelare con recipiente e spatola
1. Riempire il recipiente con cemento osseo in polvere e liquido. Assicurarsi di svuotare completamente entrambe le confezioni nel
recipiente.
2. Mescolare i componenti con l’ausilio della spatola per ottenere una massa omogenea. Questa procedura dovrebbe essere
effettuata di continuo per circa 1 minuto, per raggiungere una consistenza regolare.
b) Miscelatore per cementi ossei (SOMIX 2.0)
RIEMPIMENTO:
1. Rimuovere il tappo di chiusura del SOMIX
®
2.0 ruotandolo in senso antiorario. (1)
2. Posizionare l’imbuto centralmente sulla camera. (2)
3. Immettere per prima la polvere e poi il liquido nella camera completamente senza spargimenti. (3) Rimuovere l’imbuto.
4. Chiudere la camera ruotando il tappo in senso orario sino al suo bloccaggio. Ci sono vari indicatori sulla camera mostrano la
posizione di chiusura. (4)
MISCELAZIONE:
5. Verificare la chiusura della valvola a 2 vie sommitale. Ruotare e muovere velocemente l’impugnatura su e giù. In questo modo la
paletta interna crea una miscela omogenea all’interno della camera. (5) La miscelazione va svolta per 30-40 secondi.
Controllare l’aspetto del cemento osseo attraverso le pareti trasparenti della camera.
In caso di creazione di vuoto all’interno della camera va aperta la valvola sommitale.
TRASFERIMENTO:
6. Aprire la valvola sommitale. Ruotare l’impugnatura in senso antiorario spingendola verso l’alto. (6) Dopodiché la camera inizierà a
svuotarsi dell’aria.
7. Arrestarsi nel momento in cui il fondo della camera arriva alla base della scala graduata con ingresso del cemento nella valvola e
nel filtro. (7)
8. Rimuovere il filtro ruotandolo in senso antiorario. (8)
9. Connettere un sistema di iniezione oppure una siringa al connettore Luer-Lock. (9)
ITALIAN

19/32
10. Il cemento, ruotando ulteriormente l’impugnatura, passerà nel sistema di iniezione sino al completo riempimento. Lo stantuffo
della siringa si innalzerà automaticamente. Un rumore di 6 ‘click’ indica un giro di 360° segnalando l’avanzamento dell’operazione
di riempimento. (10)
11. Togliere la pressione di riempimento premendo il pulsante e/o chiudendo la valvola. (11)
12. Rimuovere dalla valvola, tramite rotazione antioraria, il sistema di iniezione riempito di cemento. (12)
13. Rifare la procedura da 9 a 12 sino riempimento di tutti i sistemi di iniezione col cemento disponibile.
•Date le geometrie del miscelatore, una minima quantità di cemento rimarrà nella camera e non potrà essere trasferita. Questo
non limita l’efficacia del dispositivo.
•Il cemento va trasferito nel sistema di iniezione o nella siringa nel minor tempo possibile, nella fase di bassa viscosità. A seconda
del cemento, il periodo normalmente disponibile per il trasferimento è di 2-4 minuti dalla fine della miscelazione.
•Ad ogni ‘click’ vengono trasferiti circa 0,2 cc di cemento in media.
5.3 Sistema di iniezione e iniezione
Cement Injection System (CIS
®
, Fig. 6) e Small Injection System (SIS, Fig. 7)
1. Spingere le manopole (4) una contro l’altra, tenere immersa l’apertura di aspirazione (3) nella miscela sciolta, aspirare almeno 3
ml del cemento e far uscire tutta la quantità fuori nel contenitore utilizzato per la miscelazione. In questo modo si fa uscire tutta
l’aria dal Sistema di iniezione. l’utilizzo del sistema di miscelazione i flessibili di aspirazione non sono necessari e il sistema di
iniezione comunica direttamente con un rubinetto a due vie. Infine seguire i punti 9-12 del presente manuale nel Capitolo 5.2.
2. Far aspirare nel sistema di iniezione tutta la quantità necessaria della materia. Per evitare la contemporanea aspirazione delle
bolle d’aria si consiglia tenere il contenitore per la miscelazione in posizione obliqua ed immergere fino in fondo l’apertura di
aspirazione (3) nella miscela del cemento.
3. Tutta l’aspirazione del cemento dovrebbe durare per almeno cinque secondi siccome nel caso dell’aspirazione troppo intensa si
rischia di aspirare contemporaneamente delle bolle d’aria. L’esattezza della scala graduata in ml (1) è di ±0,2 ml.
4. Estrarre il mandrino interno dalla cannula inserita. Il mandrino deve rimanere nella zona sterile siccome con l’aiuto del quale si
deve spingere il cemento dalla cannula nel corpo della vertebra.
5. Togliere l’apertura di aspirazione (3) dal pezzo girevole (2) del sistema di iniezione.
6. Avvitare a fondo alla cannula il pezzo girevole (2) del sistema di iniezione.
7. Aspettare finché il cemento non avrà la consistenza desiderata.
8. L’iniezione del cemento con l’aiuto dei raggi. Al momento, quando il cemento può essere applicato solo producendo la forza
maggiore, si deve iniziare subito con il seguente passo siccome si rischia il pericolo dell’indurimento della cannula.
Attenzione: La produzione della forza maggiore può provocare il danneggiamento meccanico del sistema Sistema di
iniezione.
9. Svitare dalla cannula la parte girevole (2) del sistema di iniezione.
10. Introdurre di nuovo il mandrino fino in fondo nella cannula e spingere fuori nel corpo della vertebra il cemento che è rimasto nella
sua cavità. La tabella dei volumi residuali delle cannule della ditta Somatex per la vertebroplastica si trovano nel relativo libretto
d’uso.
11. Durante la fase dell’indurimento del cemento girare di 360° la cannula, ripetutamente ad alcuni intervalli di tempo (30-60 sec.),
per evitare che l’ago s’incastri nel cemento indurito.
L'orario di lavoro di cemento dipende dal dispositivo dell'iniezione nell'accordo ai grafici nell'immagine. 6 e 7.
5.4. Assistenza postoperatoria
1. Dopo l’indurimento del cemento estrarre l’ago con i movimenti rotatori tirandolo con la mano fuori dal corpo della vertebra. In
base alla Fig. 2 il supporto dell’ago può essere utilizzato come ausilio per la rimozione della cannula.
2. Medicare il luogo della ferita.
6. Conservazione e Smaltimento:
Conservazione:
Conservare nel suo imballaggio originale non aperto, in un luogo buio, pulito e asciutto (umidità 30 – 65%) ad una temperatura
tra 41°F e 86° F (5°C – 30°C).
Smaltimento:
Dopo l’uso il prodotto va smaltito in osservanza delle regole di smaltimento ospedaliere.
ITALIAN

20/32
Manual de Instruçőes (Portuguese)
Este instrumento foi expressamente concebido para uma única utilização. O produto não deve ser reutilizado após a aplicação única.
A qualidade doa matérias, superfícies e juntas adesivas podem estar deterioradas. Não asseguramos uma aplicação segura. O
produto não é direccionado para processos de limpeza e esterilização após a aplicação única. A esterilidade do reprocessamento
após a utilização única não poderá ser assegurado. O risco de ferimentos incautos e de infecções, em particular infecções cruzadas
entre paciente e pessoal médico aumenta desmesuradamente. A firma Somatex declina qualquer responsabilidade em caso de uma
nova esterilização e reutilização do instrumento.
Estas declarações para o conjunto de vertebroplastia SOMATEX® NÃO têm a finalidade de estabelecer ou propor métodos médicos
ou cirúrgicos. O médico em questão é responsável por determinar o processo e os métodos apropriados para o uso deste produto.
1. Indicações:
A VERTEBROPLASTIA serve para estabilizar a estrutura do corpo vertebral com cimento ósseo para o tratamento de fraturas por
compressão do corpo vertebral patológicas e dolorosas, que não podem ser tratadas com uma terapia de tratamento da dor
conservadora e são caraterizadas por:
- Osteoporose primária e secundária,
- Osteólise de tumores no corpo vertebral (cancro metastático ou mieloma),
- Osteólise de hemangiomas vertebrais sintomáticos.
Note-se, que os procedimentos de aumento vertebral são apenas tratamentos paliativos para estabilizar o corpo vertebral e a dor.
Não tratam a doença base (osteoporose ou doenças tumorais).
A VERTEBROPLASTIA não é adequada para ser utilizada como profilaxia em pacientes com osteoporose, com ou sem fraturas
vertebrais.
2. Contraindicações
A VERTEBROPLASTIA não se aplica quando se sabe que o paciente tem hipersensibilidade aos componentes dos conjuntos e/ou a
cimento ósseo com meio de contraste.
Contraindicações absolutas:
- Gravidez ou aleitamento
- infeções locais ou sistémicas não completamente esclarecidas
- doença hemorrágica incontrolável
Contraindicações relativas:
- em tumores avançados no espaço epidural do corpo vertebral
- Tumores do corpo vertebral, que afetem o canal espinal e que apanhe mais de 20% da vértebra
- Fraturas de rutura na coluna vertebral
- danos vertebrais anatómicos, causados pelo acesso incerto para o corpo vertebral
- falta de cooperação dos pacientes, ou pacientes que não estejam em posição de seguir as instruções do pessoal de
acompanhamento médico
- Distúrbios metabólicos, que interferem com a reação de polimerização do cimento ósseo
- Osteomalacia
- infeções não locais, que potencialmente podem afetar o corpo vertebral
- Hipotensão
- Insuficiência cardíaca
- Insuficiência renal
3. Descrição do produto
(Im. 1, Invólucro)
O conjunto de VERTEBROPLASTIA da Somantex
®
é um produto de utilização única esterilizado, que serve para a injeção de
cimento ósseo através de uma agulha no corpo vertebral. Dependendo da versão, que consiste numa ou duas agulhas (1), para
punção mono ou bilateral, um porta-agulha (2) para orientar a agulha para fora do caminho do feixe, um copo de mistura com
espátula (4) ou um sistema de mistura (3) e uma ou duas pequenas seringas (SIS) (5) ou um sistema de injeção (CIS
®
) (6). Todos os
conjuntos (tabela 2) podem ser complementados com os acessórios mencionados na lista (tabela 3).
4. Avisos
- Imediatamente, durante ou após cada vertebroplastia, devem ser cuidadosamente monitorizadas as alterações na pressão
arterial do paciente. Durante o tratamento de reposição, podem ocorrer reações adversas do sistema cardiovascular dos
pacientes. As reações de hipotensão podem ocorrer entre 5 segundos ou vários minutos após a última aplicação de cimento
ósseo. Em casos raros, pode levar a paragem cardíaca. Por esse motivo, os pacientes deve ser cuidadosamente monitorizados
imediatamente após a utilização de cimento ósseo, no que diz respeito às funções vitais.
- Em casos raros, têm ocorrido relacionados com uma vertebroplastia, efeitos secundários graves, como enfarte do miocárdio,
paragem cardíaca, acidente vascular cerebral e embolia pulmonar.
- No caso de complicações com os pulmões, coração ou sistema circulatório, é necessário produzir novamente uma condição
controlada e uma volumina razoável.
- No caso de problema respiratório agudo ou insuficiência cardíaca ou reanimação, devem ser fornecidas técnicas adequadas
para a manutenção das funções vitais.
- Antes da implantação do cimento ósseo, é necessário eliminar os riscos ou as contraindicações. (ver também as
contraindicações absolutas ou relativas). Em específico, deve ser realizado um controlo preciso da morfologia do corpo vertebral
fraturado, a vascularização possível ou a presença de edema por procedimentos de imagem apropriados.
- Antes da vertebroplastia, devem ser criadas medidas de proteção, para corrigir imediatamente quaisquer complicações devidas
à cirurgia.
- A punção do osso com a agulha da vertebroplastia deve ser realizada através de um procedimento de imagem adequado, para
verificar o posicionamento correto da ponta da agulha.
- É absolutamente necessário realizar o aumento vertebral em condições em tempo real, com fluoroscopia e raio-X, para observar
a distribuição de cimento ósseo em toda a extensão do corpo vertebral e para o utilizador evitar o vazamento de cimento para
fora do corpo vertebral.
PORTUGUESE
Table of contents
Languages:
Other Somatex Medical Equipment manuals

Somatex
Somatex TUMARK Professional User manual

Somatex
Somatex Tumark MRI User manual
Somatex
Somatex Tumark Eye User manual

Somatex
Somatex SurgLite SL0200-15 User manual
Somatex
Somatex Tumark Q User manual

Somatex
Somatex Tumark Vision User manual

Somatex
Somatex Tumark Vision MRI User manual

Somatex
Somatex CT-Eye-ProteX User manual
Popular Medical Equipment manuals by other brands

Getinge
Getinge Arjohuntleigh Nimbus 3 Professional Instructions for use

Mettler Electronics
Mettler Electronics Sonicator 730 Maintenance manual

Pressalit Care
Pressalit Care R1100 Mounting instruction

Denas MS
Denas MS DENAS-T operating manual

bort medical
bort medical ActiveColor quick guide

AccuVein
AccuVein AV400 user manual











