es
Aesculap®
Instrumentos de vástago tubular
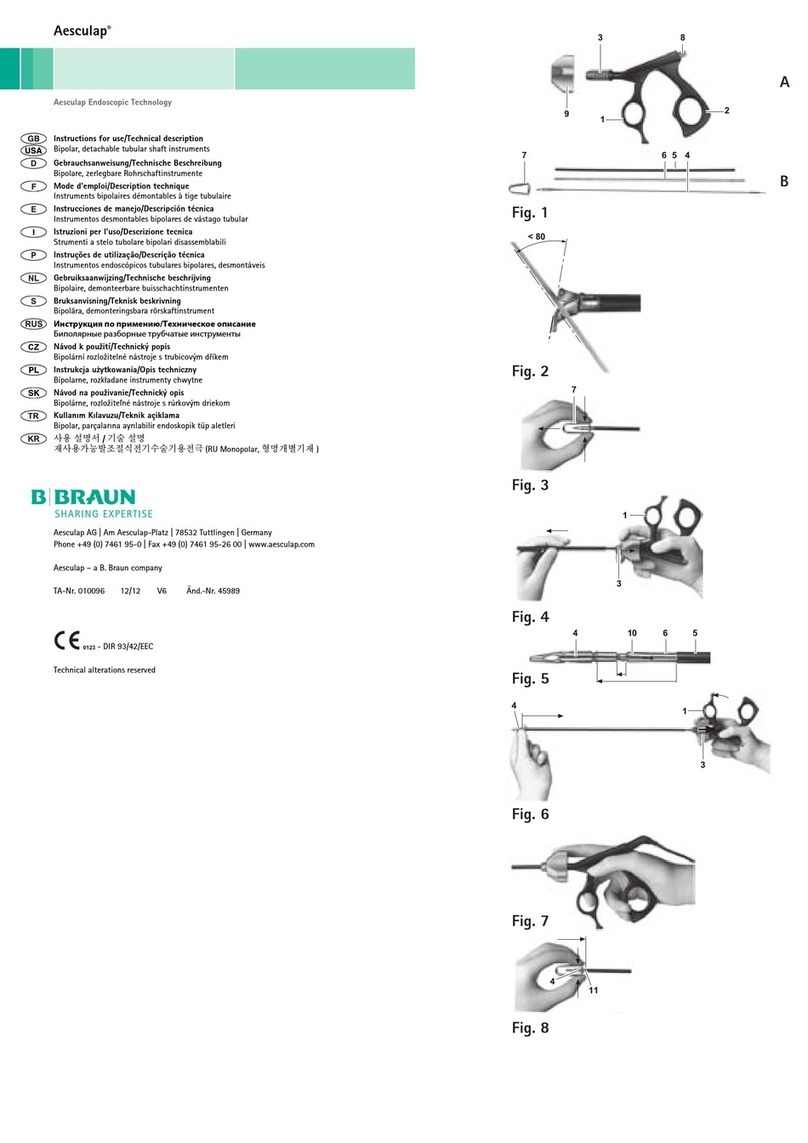
Leyenda
1Estrella giratoria
2Mango
3Botón
4Parte móvil del mango
5Vástago completo (tubo exterior, tubo interior, pieza de trabajo)
6Pieza boca
7Pieza de trabajo
8Lengüetas flexibles
9Tubo interior
10 Tubo exterior
11 Elementos elásticos (aviso táctil)
Símbolos en el producto y envase
1. Finalidad de uso
Los instrumentos desmontables de vástago tubular se emplean, en función del diseño del extremo de trabajo, para
cortar, preparar, sujetar y extraer fragmentos de biopsias.
Se introducen en el cuerpo con la ayuda de un instrumento de abordaje (p. ej. trocar).
2. Indicaciones
Indicaciones, ver Finalidad de uso.
Nota
El fabricante no se hace responsable de un uso del producto contrario a las indicaciones mencionadas y/o las aplica-
ciones descritas.
3. Contraindicaciones
3.1 Contraindicaciones absolutas
No se han descrito.
3.2 Contraindicaciones relativas
De acuerdo con nuestros conocimientos actuales, no existen contraindicaciones relativas específicas del producto.
Sin embargo, existen condiciones médicas o quirúrgicas que pueden alterar la técnica endoscópica, como hemorra-
gias graves, que pueden limitar la visibilidad en el campo quirúrgico.
En caso de contraindicaciones relativas, el usuario deberá tomar una decisión individual sobre el uso del producto.
4. Riesgos y efectos secundarios
En el marco de la obligación de informar reglamentariamente, se destacan los siguientes posibles riesgos y efectos
secundarios conocidos por el fabricante relacionados con el uso de instrumental quirúrgico. Son principalmente
específicos de un procedimiento, no específicos de un producto, e incluyen daños adversos en el tejido circundante
que pueden provocar, por ejemplo, hemorragias, infecciones o incompatibilidades de los materiales o partes del ins-
trumental que queden sin atención en el paciente.
5. Manipulación correcta y preparación
►Confiar la aplicación y el uso del producto y de los accesorios exclusivamente a personal con la formación reque-
rida para ello o que disponga de los conocimientos o experiencia necesarios.
►Seguir las instrucciones del producto y conservarlas como referencia.
►Utilizar el producto sólo de acuerdo con su finalidad de uso, ver Finalidad de uso.
►Limpiar a mano o a máquina el producto nuevo de fábrica después de haberlo desembalado y antes de la primera
esterilización.
►Conservar el producto nuevo de fábrica o no utilizado aún en un lugar seco, limpio y protegido.
►Antes de cada uso, comprobar visualmente que el producto no presente: piezas sueltas, deformadas, rotas, agrie-
tadas, desgastadas ni fragmentadas.
►No utilizar ningún producto dañado o defectuoso. Retirar inmediatamente el producto si está dañado.
►Sustituir inmediatamente por una pieza de recambio original cualquier componente que esté dañado.
►Para evitar que el extremo de trabajo se dañe: introducir el producto con cuidado en el canal de trabajo (p. ej.,
trocar)
►Para trabajar mediante sistema bi-instrumental con instrumentos AF en el interior de un trocar: cuando se pueda,
introducir primero el instrumento de vástago tubular para evitar lesiones con el aislamiento de AF. Al introducir
el instrumento: cuando sea posible, retirar primero el instrumento AF.
6. Manejo del producto
ADVERTENCIA
Peligro de lesiones y/o fallos de funcionamiento.
►Comprobar el funcionamiento antes de cada uso.
ADVERTENCIA
Peligro de lesiones y/o fallos de funcionamiento.
►Utilizar los instrumentos FF385R FF389R sólo con el trocar FF399R.
ADVERTENCIA
Peligro de lesiones si se utiliza el producto fuera del campo visual.
►Utilizar el producto sólo bajo control visual.
Nota
Los elementos elásticos envían un aviso táctil al usuario, antes de que el instrumento salga del trocar FF399R y entre
en el área quirúrgica. La función de aviso táctil sólo se puede garantizar si se utiliza el trocar FF399R.
7. Desmontaje
Los instrumentos de vástago tubular se desmontan en las siguientes piezas:
■Mango 2
■Tubo exterior 10
■Tubo interior 9
■Pieza de trabajo 7
►Separar el mango 2y la pieza de trabajo 7, ver Fig. 1:
– Abrir completamente la parte móvil del mango 4.
– Presionar el botón 3y mantenerlo presionado.
– Simultáneamente tirar hacia abajo la pieza móvil del mango 4.
►Separar el vástago 5y el mango 2, ver Fig. 2:
– Retirar la estrella giratoria 1en dirección al mango 2hasta el tope.
– Sujetar la estrella giratoria 1 en el tope y extraer el vástago 5.
►Desmontar el vástago 5, ver Fig. 3:
– Retirar el tubo exterior 10 y el tubo interior 9de la pieza de trabajo 7.
– Extraer el tubo interior 9de la pieza de trabajo 7, ver Fig. 4.
8. Montaje
►Montaje del vástago 5, ver Fig. 5:
– Desplazar el tubo interior 9con las lengüetas elásticas 8hacia el extremo de trabajo de la pieza de trabajo 7
hasta que las lengüetas elásticas 8encajen.
– Deslizar el tubo exterior 10 hasta el tope sobre el tubo interior 9de la pieza de trabajo 7. Para ello, asegu-
rarse de que las flechas de la marca circundante señalan hacia el mango, ver Fig. 6.
►Unir el vástago 5y el mango 2:
– Asegurarse de que el tubo exterior 10 se ha deslizado hasta el tope sobre el tubo interior 9con la pieza de
trabajo 7, ver Fig. 7.
– Retirar la estrella orientable 1hasta el tope y mantenerla en esa posición, ver Fig. 8.
– Sujetar el vástago 5en el extremo de trabajo cerrado.
– Girar ligeramente el vástago 5y el mango 2al insertarlos, hasta que queden unidos.
– Dejar que la estrella giratoria 1se deslice hacia delante, ver Fig. 9. Asegurarse de que el vástago 5está bien
encajado en la empuñadura 2y no se suelta aunque se tire de él.
►Unir completamente el mango 2y el vástago 5:
– Abrir completamente el mango 2.
– Deslizar hacia arriba el mango 4, sujetando al mismo tiempo la pieza de trabajo 7, hasta que encaje el
botón 3, ver Fig. 10.
– Comprobar que la pieza móvil del mango 4queda correctamente fijada.
►Comprobar el funcionamiento del producto:
– Abrir y cerrar completamente el instrumento.
– Girar la estrella giratoria 1para comprobar la rotación.
9. Proceso homologado del tratamiento de instrumental quirúrgico
9.1 Advertencias de seguridad generales
Nota
Cumplir las disposiciones legales y las normas y directrices nacionales e internacionales, además de las normas higié-
nicas del centro donde se va a llevar a cabo el tratamiento de los productos.
Nota
En el caso de pacientes que padezcan la enfermedad de Creutzfeldt-Jakob, o con sospecha de padecer dicha enferme-
dad o sus variantes, deberá cumplirse la normativa vigente del país en cada caso con respecto al tratamiento de los
productos
Nota
Deberá tenerse en cuenta que la correcta limpieza de este producto sanitario sólo podrá ser garantizada mediante una
validación previa del proceso de tratamiento. La responsabilidad corresponde al usuario/preparador.
Para la validación se han utilizado las sustancias químicas indicadas.
9.2 Indicaciones generales
Los restos de intervenciones quirúrgicas que se hayan secado o fijado pueden dificultar o impedir la limpieza y pro-
vocar corrosión. Por lo tanto, entre el uso y el acondicionamiento no se deberá superar un periodo de 1 h, no se debe-
rán utilizar temperaturas de prelavado superiores a 45 °C y no se deberán utilizar desinfectantes fijados (principios
activos: aldehído y alcohol).
Una dosis excesiva de agentes neutralizantes o disolventes puede provocar agresiones químicas y/o decoloración, así
como la ilegibilidad visual o automática de las inscripciones de láser en el acero inoxidable.
En el caso de productos de acero inoxidable, los restos de cloro y sustancias cloradas (p. ej., los contenidos en residuos
de intervenciones quirúrgicas, fármacos, soluciones salinas, agua para limpieza, desinfección y esterilización) pueden
provocar daños irreversibles por corrosión (corrosión por picaduras, corrosión interna) en dichos productos y acabar
destruyéndolos. Para eliminar cualquier resto, deberán aclararse a fondo los productos con agua completamente des-
mineralizada, secándolos a continuación.
Efectuar un secado final, si es necesario.
Se deben utilizar únicamente productos químicos de proceso comprobado y autorizado (p. ej., autorizados por
VAH/DGHM o la FDA, o con marcado CE), y recomendados por el fabricante en cuanto a su compatibilidad con el
material. Deberán cumplirse estrictamente todas las instrucciones del fabricante para el producto químico. De lo
contrario, pueden surgir los siguientes problemas:
■Daños en el material como corrosión, grietas, roturas, envejecimiento prematuro o hinchamiento.
►No limpiar nunca la superficie con cepillos metálicos u otros agentes abrasivos, ya que existe peligro de corrosión.
►Para obtener más información sobre una esterilización y limpieza higiénica, segura y respetuosa con los mate-
riales, consulte www.a-k-i.org sección "AKI-Brochures", "Red brochure".
9.3 Productos reutilizables
No se conocen efectos de la fabricación que puedan provocar daños en el producto.
El producto se puede reutilizar un máximo de 75 veces, siempre que se utilice con cuidado y esté limpio y no presente
daños. Cualquier reutilización más allá de lo descrito se realizará bajo responsabilidad del usuario.
Una inspección visual y funcional antes del siguiente uso es la mejor forma de reconocer un producto que ya no
funciona.
9.4 Desmontaje del producto antes de comenzar el proceso de tratamiento
►Desmontar el producto inmediatamente después de su uso siguiendo las instrucciones.
►Abrir los productos articulados.
9.5 Preparación en el lugar de uso
►En su caso, limpie las superficies que no estén a la vista, preferentemente con agua totalmente desalinizada, p. ej.
con una jeringa de un solo uso.
►Eliminar por completo con un paño húmedo que no deje pelusa los restos visibles de intervenciones quirúrgicas.
►Transportar el producto mojado en el contenedor de eliminación cerrado en un plazo máximo de 1 h para su lim-
pieza y desinfección.
9.6 Preparación previa a la limpieza
►Desmontar el producto antes de la limpieza, ver Desmontaje.
Atención, señal de advertencia general
Atención, observar la documentación adjunta